
 .
. +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$ +HCl.
+HCl. 分析 a、b、c、d代表四种短周期主族元素,a、b、c同周期,且原子序数之和为22,元素b的最简单氢化物与元素a的氢化物可化合成离子化合物M,则M为铵盐,b的最高和最低化合价的代数和为2,则b为N元素;可知a为F元素,M为NH4F,c的原子序数为22-7-9=6,故c为C元素;d是短周期中金属性最强的元素,则d为Na,据此解答.
解答 解:a、b、c、d代表四种短周期主族元素,a、b、c同周期,且原子序数之和为22,元素b的最简单氢化物与元素a的氢化物可化合成离子化合物M,则M为铵盐,b的最高和最低化合价的代数和为2,则b为N元素;可知a为F元素,M为NH4F,c的原子序数为22-7-9=6,故c为C元素;d是短周期中金属性最强的元素,则d为Na.
(1)由上述分析可知,a为F元素、b为N元素、c为C元素,d在氧气中燃烧生成Na2O2,电子式为 ,
,
故答案为:F;N;C; ;
;
(2)M为NH4F,铵根离子与氢氧根离子结合不能电离共存,故答案为:OH-;
(3)元素e为a的同主族短周期元素,则e为Cl,氯气与水反应生成HCl与HClO,反应的离子方程式为:,故答案为:Cl2+H2O=H++Cl-+HClO;
(4)c的一种氢化物的相对分子质量为78,分子中两种元素的原子个数比为1:1,分子中C、H原子数目为$\frac{78}{12+1}$=6,故分子式为C6H6,C6H6分子为平面结构,分子中有12个原子共平面,该氢化物与氯气质在氯化铁催化作用下发生取代反应的化学方程式: +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$ +HCl,
+HCl,
故答案为:12; +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$ +HCl.
+HCl.
点评 本题考查结构性质位置关系应用,氢化物之间形成盐是推断突破口,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 该原子的质量数为222 | B. | Rn是86号元素 | ||
| C. | 一个222 86Rn原子中有136个中子 | D. | 一个222 86Rn原子中有136个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沸点/℃ | 密度(g.cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.5 | 0.8107 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A.元素原子的核外p电子总数比s电子总数少1 |
| B.元素价电子排布式为nsnnp2n |
| C.元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| D.原子核外所有p轨道全满或半满 |
| E.元素的主族序数与周期数的差为4 |
| F.是前四周期中电负性最小的元素 |

 ;1mol B22+中含有的π键数目为2NA.
;1mol B22+中含有的π键数目为2NA.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝锂合金是铝与锂形成的一种化合物 | |
| B. | 锂是碱金属元素,性质活泼,铝锂合金与水反应生成氢气 | |
| C. | 铝离子和锂离子的核外电子排布相同 | |
| D. | 若铝锂合金中锂含量为1.1%,则127.3g铝锂合金中含有锂原子0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
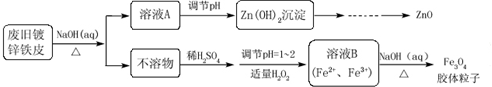
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com