
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的漂白剂。Na2S2O4易溶于水,难溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。回答下列问题:
(1)Na2S2O4在潮湿空气中氧化,生成的两种常见酸式盐是___(填化学式)。
(2)锌粉法制备Na2S2O4的工艺流程如图所示:
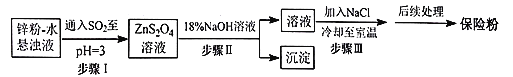
①工业上常将锌块进行预处理得到锌粉-水悬浊液,其目的是__。
②步骤Ⅰ中发生反应的化学方程式为__。
③在步骤Ⅲ中得到的Na2S2O4固体要用乙醇洗涤,其优点是__,“后续处理”最终要加入少量的Na2CO3固体,其原因是__。
(3)目前,我国普遍采用甲酸钠法生产连二亚硫酸钠,其原理是先将HCOONa和烧碱加入乙醇水溶液中,然后通入SO2发生反应,有CO2气体放出,总反应的离子方程式是___。
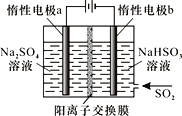
(4)有人设计了图示方法同时制备连二亚硫酸钠和过二硫酸钠(Na2S2O8),并获得中国专利。电解过程中,阴极室生成Na2S2O4,a极的电极反应式为__,通过阳离子交换膜的离子主要是Na+,其迁移方向是__(填“a到b”或“b到a”)。
【答案】NaHSO3和NaHSO4 增大锌粒的表面积,加快化学反应速率 Zn+2SO2=ZnS2O4 减少Na2S2O4的溶解损失,易于干燥 Na2CO3为碱性物质,“保险粉”在碱性介质中较稳定 HCOO-+OH-+2SO2=S2O42-+CO2+H2O 2SO42--2e-=S2O82- a到b
【解析】
(1)Na2S2O4中S显+4价,在潮湿空气中氧化,S转化为+6价,则生成的两种常见酸式盐应为硫酸和亚硫酸的酸式盐。
(2)①将锌块进行预处理得到锌粉-水悬浊液,可以增大其与SO2的接触面积。
②步骤Ⅰ中,锌与SO2在水溶液中发生反应,生成ZnS2O4。
③Na2S2O4固体易溶于水,难溶于乙醇,用乙醇洗涤,从溶解和干燥两个方面寻找原因;Na2S2O4在碱性介质中较稳定,Na2CO3固体可提供碱性环境。
(3)HCOONa、烧碱、SO2发生反应,生成Na2S2O4、CO2等,由此可写出反应的离子方程式。
(4)a极的电解质为SO42-,由题意知,它将转化为S2O82-,由此可得出电极反应式;通过阳离子交换膜的离子主要是Na+,从电荷守恒出发可确定其迁移方向。
(1)Na2S2O4中S显+4价,在潮湿空气中被氧化,S部分转化为+6价,则生成的两种常见酸式盐为NaHSO3和NaHSO4。答案为:NaHSO3和NaHSO4;
(2)①锌粉-水悬浊液与SO2的接触面积比锌粉与SO2的接触面积大,反应速率快。答案为:增大锌粒的表面积,加快化学反应速率;
②步骤Ⅰ中,锌与SO2在水溶液中发生反应,生成ZnS2O4,反应的化学方程式为Zn+2SO2=ZnS2O4。答案为:Zn+2SO2=ZnS2O4;
③Na2S2O4固体易溶于水,难溶于乙醇,用乙醇洗涤,既可减少溶解损失,又易于干燥;Na2S2O4在碱性介质中较稳定,Na2CO3固体可提供碱性环境,增强“保险粉”的稳定性。答案为:减少Na2S2O4的溶解损失,易于干燥;Na2CO3为碱性物质,“保险粉”在碱性介质中较稳定;
(3)HCOONa、烧碱、SO2发生反应,生成Na2S2O4、CO2等,反应的离子方程式为HCOO-+OH-+2SO2=S2O42-+CO2+H2O。答案为:HCOO-+OH-+2SO2=S2O42-+CO2+H2O;
(4)a极的电解质为SO42-,由题意知,它将转化为S2O82-,电极反应式为2SO42--2e-=S2O82-;通过阳离子交换膜的离子主要是Na+,电极反应发生后,阳极Na+富余,它应向阴极迁移,所以Na+的迁移方向是由a到b。答案为:2SO42--2e-=S2O82-;a到b。


科目:高中化学 来源: 题型:
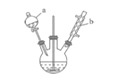
【题目】苯甲醛是一种重要的化工原料,某小组同学利用如图所示实验装置(夹持装置已略去)制备苯甲醛。
已知有机物的相关数据如下表所示:
有机物 | 沸点℃ | 密度为g/cm3 | 相对分子质量 | 溶解性 |
苯甲醛 | 178.1 | 1.04 | 106 | 微溶于水,易溶于乙醇、醚和卤代烃 |
苯甲醇 | 205.7 | 1.04 | 108 | 微溶于水,易溶于乙醇、醚和卤代烃 |
二氯甲烷 | 39.8 | 1.33 | 难溶于水,易溶于有机溶剂 |
实验步骤:
①向容积为500mL的三颈烧瓶加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9-10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。
请回答下列问题:
(1)仪器b的名称为______,搅拌器的作用是______。
(2)苯甲醇与NaClO反应的化学方程式为_______。
(3)步骤①中,投料时,次氯酸钠不能过量太多,原因是____;步骤③中加入无水硫酸镁,若省略该操作, 可能造成的后果是______。
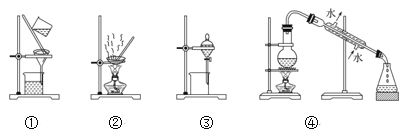
(4)步骤②中,应选用的实验装置是___(填序号),该操作中分离出有机相的具体操作方法是___。
(5)步骤④中,蒸馏温度应控制在_______左右。
(6)本实验中,苯甲醛的产率为________(保留到小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图甲是一种在微生物作用下将废水中的尿素CO(NH2)2转化为环境友好物质,实现化学能转化为电能的装置,并利用甲、乙两装置实现在铁上镀铜。下列说法中不正确的是

A. 乙装置中溶液颜色不变
B. 铜电极应与Y相连接
C. M电极反应式:CO(NH2)2+H2O-6e-=CO2↑+N2↑+6H+
D. 当N电极消耗0.25 mol气体时,铜电极质量减少16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环与环之间共用两个或多个碳原子的多环烷烃称为桥环烷烃,其中二环[1.1.0]丁烷 (![]() )是其中一种。下列关于该化合物的说法正确的是
)是其中一种。下列关于该化合物的说法正确的是
A. 与C3H4是同系物
B. 一氯代物只有一种
C. 与环丁烯互为同分异构体
D. 所有碳原子可能都处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在20 mL 0.1 mol·L-1一元弱酸HA溶液中滴加0. 1 mol· L-1 NaOH溶液,溶液中1g[c(A-)/c(HA)]与pH关系如图所示。下列说法正确的是

A. A点对应溶液中:c(Na+)>c(A-)>c(H+)>c(OH-)
B. 25℃时,HA酸的电离常数为1. 0× 10-5.3
C. B点对应的NaOH溶液体积为10 mL
D. 对C点溶液加热(不考虑挥发),则c(A-)/[c(HA)c(OH-)]一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来食品安全问题成为社会各界日益关注的焦点话题.香港地区食环署食物安全中心曾对十五个桂花鱼样本进行化验,结果发现十一个样本中含有孔雀石绿。孔雀石绿是化工产品,具有较高毒性,高残留,且长期服用后,容易致癌、致畸,对人体有害。其结构简式如图所示。下列关于孔雀石绿的说法正确的是( )

A.孔雀石绿的分子式为C23H25N2
B.1mol孔雀石绿在一定条件下最多可与6molH2发生加成反应
C.孔雀石绿属于芳香烃
D.孔雀石绿苯环上的一氯取代物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组用图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
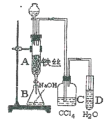
(1)写出A中反应的化学方程式_______________。
(2)观察到A中的现象是_____________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________,写出有关的化学方程式______________________________。
(4)C中盛放CCl4的作用是________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_______,现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,能说明化学平衡一定向正反应方向移动的是( )
A. N2O4(g)![]() 2NO2(g),改变某一条件后,气体颜色加深
2NO2(g),改变某一条件后,气体颜色加深
B. H2(g)+I2(g)![]() 2HI(g),单位时间内消耗H2和HI的物质的量之比大于1:2
2HI(g),单位时间内消耗H2和HI的物质的量之比大于1:2
C. N2(g)+3H2(g) ![]() 2NH3(g),改变某一条件后,NH3的体积分数增加
2NH3(g),改变某一条件后,NH3的体积分数增加
D. 2SO2(g) +O2(g)![]() 2SO3(g),恒温恒压条件下,充入He
2SO3(g),恒温恒压条件下,充入He
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种清洁、高效新能源, 也是重要的化工原料。
(1)通过热化学循环在较低温度下由硫化氢分解制备氢气的反应系统原理为:
SO2(g)+I2(s)+2H2O(l)=2HI(aq)+H2SO4(aq) H1=-151kJmol-1
2HI(aq)=H2(g)+I2(s) H2=+110kJmol-1
H2S(g)+H2SO4(aq)=S(s)+SO2(g)+2H2O(l) H3=+61kJmol-1
(热化学硫碘循环硫化氢分解联产氢气、硫磺系统)
通过计算可知,该系统制氢的热化学方程式为___________。
(2)工业上利用CO和H2合成清洁能源CH3OH,其反应为CO(g)+2H2(g)CH3OH(g)ΔH= -116 kJ·mol-1。如图表示CO的平衡转化率(α)随温度和压强变化的示意图:
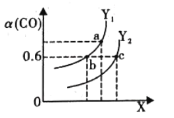
①X 表示的是______ (填“温度”或“压强”) ,理由是_________;Y1______Y2 (填“<”、“ >”或“=”)
②在2L恒容密闭容器中充入2 mol CO 和4 mol H2,一定条件下经过10 min 达到平衡状态c 点处。在该条件下,从开始至达到平衡状态v(CH3OH) =______ molL-1min -1,平衡常数K=________(填最简分数)。平衡常数Ka、Kb、Kc的大小关系是______
③下列措施既能增大反应速率又能提高反应物转化率的是______ (填字母)。
A. 使用催化剂 B. 及时分离CH3OH C.升高温度 D.增大压强
(3) 已知燃料电池的比能最与单位质量燃料物质失去的电子数成正比。理论上H2、CH4、CH3OH的碱性电池的比能量由大到小的顺序为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com