
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式 。
(2)整个过程中的还原剂是 。
(3)把KI换成KBr,则CCl4层变为 色;继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
(4)加碘盐中含碘量为20~50 mg·kg-1。制取加碘盐(含KIO3的食盐)1 000 kg,若用KI与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)。
(1)I2+5Cl2+6H2O=2HIO3+10HCl
(2)KI、I2 (3)红棕 HBrO3>Cl2>HIO3 (4)10.58
【解析】(1)CCl4层变成紫色说明有I2生成,继续滴加氯水变成无色,说明I2又被氧化生成HIO3,同时生成HCl。(2)首先KI被氧化生成I2,后来I2又被氧化生成KIO3,所以整个过程中的还原剂是KI、I2。(3)Br2的CCl4溶液显红棕色;继续滴加氯水,CCl4层颜色没有变化,说明氯水能氧化I2但不能氧化Br2,结合第(1)问可得氧化性HBrO3>Cl2>HIO3。(4)KI被Cl2氧化成KIO3,对应关系式为
I- ~ KIO3 ~ 3Cl2
1 mol 3 mol
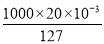 mol n(Cl2)
mol n(Cl2)
则n(Cl2)=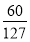 mol,V(Cl2)=
mol,V(Cl2)=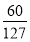 mol×22.4 L·mol-1≈10.58 L。
mol×22.4 L·mol-1≈10.58 L。


科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-2练习卷(解析版) 题型:选择题
有一混合溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32—、SO42—,现取三份100 mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生;
(2)第二份加入足量NaOH溶液加热后,收集到气体0.06 mol;
(3)第三份加入足量BaCl2溶液后,所得沉淀经洗涤、干燥、称量为6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是( )
A.K+一定存在
B.100 mL溶液中含0.01 mol CO32—
C.Cl-可能存在
D.Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-2练习卷(解析版) 题型:填空题
(1)由三个原子构成的某气体分子,其摩尔质量为M g/mol,该气体的体积为V L(标准
状况),设阿伏加德罗常数的值为NA,则:
①该气体的物质的量为________mol;
②该气体中所含的原子总数为________个;
③该气体在标准状况下的密度为________g/L;
④该气体的一个分子的质量为________g。
(2)气体化合物A分子式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为________,推断的依据为______________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-1练习卷(解析版) 题型:选择题
某无色溶液中含有大量Na2SO4、Na2CO3、NaOH,为验证其中所含的阴离子,若限定只取一次待测液,则加入试剂顺序正确的是( )
A.酚酞、BaCl2、盐酸 B.BaCl2、盐酸、酚酞
C.BaCl2、酚酞、盐酸 D.酚酞、盐酸、BaCl2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-1练习卷(解析版) 题型:选择题
下列由相关实验现象所推出的结论正确的是( )
A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性
B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42—
C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应
D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习2-3-2氧化还原反应方程式配平及计算练习卷(解析版) 题型:选择题
已知OCN-中每种元素都满足8电子稳定结构,在反应OCN-+OH-+Cl2―→CO2+N2+Cl-+H2O(未配平)中,如果有6 mol Cl2完全反应,则被氧化的OCN-的物质的量是 ( )。
A.2 mol B.3 mol C.4 mol D.6 mol
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型四 离子反应型专题练习卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.小苏打溶液中加入少量石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O
B.稀硝酸中加入少量铁粉:Fe+2H++NO3-=Fe3++NO↑+H2O
C.溴化亚铁溶液中通入足量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-

查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十四 定量计算型专题练习卷(解析版) 题型:选择题
将一定量的氯气通入30 mL浓度为10.00 mol·L-1的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是( )
A.与NaOH反应的氯气一定为0.3 mol
B.n(Na+)∶n(Cl-)可能为7∶3
C.若反应中转移的电子为n mol,则0.15<n<0.25
D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十一 图像分析型专题练习卷(解析版) 题型:选择题
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表。以下推断正确的是( )
氢氧化物 | 溶液pH | |||
开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.4 | - | - |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |

A.C点的沉淀为Fe(OH)3
B.OA段可能发生的反应有:3Ba2++6OH-+3SO42-+2Fe3+=3BaSO4↓+2Fe(OH)3↓
C.AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-=2BaSO4↓+Al(OH)3↓
D.据图计算原溶液中c(Cl-)>c(SO42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com