
【题目】如图:A处通入氯气.打开B阀时,C处红色布条无变化,关闭B阀时,C处干燥的红色布条褪色.由此作出的判断正确的是( ) 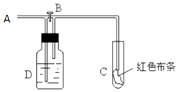
a.D中不可能是浓硫酸 b.D中可以是少量水
c.通入的氯气含有水蒸气 d.D中可以是饱和食盐水.
A.abc
B.bcd
C.abd
D.abcd
【答案】C
【解析】解:A处通入氯气.打开B阀时,C处红色布条无变化,说明氯气中不含有水蒸气,遇到有色布条不褪色,关闭B阀时,C处红色布条褪色.氯气通过D装置后,氯气和水反应生成次氯酸起漂白作用,说明D装置中的液体可以是水或水溶液,a、D中是浓硫酸吸收氯气中的水蒸气,干燥的氯气不能使干燥的红色布条褪色,故a正确;
b、D中是水时,会使有色布条褪色,故b正确;
c、实验现象说明通入的氯气不含有水分,故c错误;
d、D中可以是饱和食盐水,氯气通过后会含有水蒸气,遇到有色布条褪色,因为氯气含水蒸气,反应生成次氯酸起漂白作用,故d正确;
故abd正确,
故选C.
【考点精析】掌握氯气的化学性质是解答本题的根本,需要知道氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:
【题目】如图装置中,溶液体积均为200 ml ,开始时,电解质溶液的浓度均为0.1 mol·L-1 ,工作一段时间后,测得导线上通过了0.02 mol 电子,若不考虑溶液体积的变化,下列叙述中正确的是( )

A. (1)、(2)两装置均为电解池
B. (1)、(2)溶液的PH均减小
C. (1)中阳极电极反应式为:4OH--4e-===2H2O+O2↑
D. (1)中阴极上析出0.32 g Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室迅速制备少量氯气可利用如下反应:KMnO4+HCl→KCl+MnCl2+Cl2+H2O(未配平)此反应不需要加热,常温下就可以迅速进行,而对盐酸浓度要求不高.结合本题,回答下列问题.
(1)上述反应中被氧化的物质是 , 还原产物是 .
(2)当反应有22.4LCl2(标准状况下)生成时,转移的电子的物质的量为 .
(3)Fe2+也能使KMnO4反应生成MnCl2 , 可推测Fe2+具有 . (填“氧化性”或“还原性”)
(4)如果该反应方程式中KMnO4和MnCl2的系数都是2,则HCl的系数是 .
(5)另知反应Cl2+2I﹣=I2+2Cl﹣ , 请按照氧化性由强到弱的顺序排列I2、Cl2、KMnO4三种物质: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释物质用途或现象的反应方程式不准确的是
A. 硫酸型酸雨的形成会涉及反应2H2SO3+O2![]() 2H2SO4
2H2SO4
B. 工业上制取粗硅的化学方程式:SiO2+C![]() Si+CO2↑
Si+CO2↑
C. Na2S2O3溶液中加入稀硫酸:S2O32-+2H+=SO2+S↓+H2O
D. 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+=Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. SiO2是酸性氧化物,它不溶于水也不溶于任何酸
B. 木材浸过水玻璃后,具有防腐蚀性能且不易着火
C. 因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强
D. 氯气泄漏后,人应逆风且往低处跑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把含硫酸铵和硝酸铵的混合液a L分成两等份.一份加入含b mol NaOH的溶液并加热,恰好把NH3全部赶出;另一份需消耗c mol BaCl2才能使SO42﹣完全沉淀,则原溶液中NO3﹣的物质的量浓度为( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人体不可缺少的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:在溶液中 KIO3+5KI+3H2SO4═3I2+3H2O+3K2SO4
(1)用双线桥表示该反应中电子转移的方向和数目________,该反应中还原产物与氧化产物的物质的量比是____,0.2mol KIO3参加反应时转移电子____mol。
(2)实验结束后分离I2和K2SO4溶液所用的试剂是_______。
A.CCl4 B.酒精 C.Na2SO4溶液 D.食盐水
所用的分离方法是______,所用主要玻璃仪器是_____________。
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制1mol/L的稀硫酸溶液480mL,需用18mol/L浓H2SO4____mL,配制中需要用到的主要玻璃仪器是(填序号)______。
(4)A.100mL量筒 B.托盘天平 C.玻璃棒 D.100mL容量瓶 E.50mL 量筒 F.胶头滴管 G.烧杯 H.500mL容量瓶
(5)下面操作造成所配稀硫酸溶液浓度偏高的是______________
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”以烧酒复烧二次..... 价值数倍也。”这里用到的实验方法可用于分离
A. 酒精和水 B. 苯和水 C. 食盐水和泥沙 D. 硝酸钾和氯化钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com