
 某同学欲做1-氯丁烷的水解实验,并检验其中的氯元素.实验过程如下:(如图所示)在大试管中加入5mL 1mol•L-1 NaOH溶液和5mL的1-氯丁烷(1-氯丁烷的沸点为77~78℃,密度为0.886g•cm-3,易燃).水浴加热该试管10min以上,并控制加热温度在70~80℃.取两支小试管,各加入约1mL由2%的AgNO3和3mol•L-1硝酸按1:1比例组成的混合溶液,用胶头滴管吸取加热后大试管内的上层溶液,将此待测液逐滴加入其中一支小试管中,与另一支未加待测液的小试管内溶液相比,有白色的浑浊物出现,说明1-氯丁烷与NaOH溶液反应有Cl-生成,从而证明了1-氯丁烷中含有氯元素.请回答:
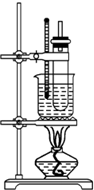
某同学欲做1-氯丁烷的水解实验,并检验其中的氯元素.实验过程如下:(如图所示)在大试管中加入5mL 1mol•L-1 NaOH溶液和5mL的1-氯丁烷(1-氯丁烷的沸点为77~78℃,密度为0.886g•cm-3,易燃).水浴加热该试管10min以上,并控制加热温度在70~80℃.取两支小试管,各加入约1mL由2%的AgNO3和3mol•L-1硝酸按1:1比例组成的混合溶液,用胶头滴管吸取加热后大试管内的上层溶液,将此待测液逐滴加入其中一支小试管中,与另一支未加待测液的小试管内溶液相比,有白色的浑浊物出现,说明1-氯丁烷与NaOH溶液反应有Cl-生成,从而证明了1-氯丁烷中含有氯元素.请回答:分析 1-氯丁烷在氢氧化钠水溶液中加热条件下可发生水解,因沸点为77~78℃,则应控制加热温度,可用水浴加热的方法,且加热温度在70~80℃,试管上方的玻璃导管起到导气、冷凝回流的作用,水解生成氯离子,可加入硝酸酸化,滴加硝酸银溶液检验,如变浑浊,可说明水解生成氯离子,以此解答该题.
解答 解:(1)1-氯丁烷在碱性条件下水解生成1-丁醇,方程式为CH3CH2CH2CH2Cl+NaOH$→_{△}^{H_{2}O}$CH3CH2CH2CH2OH+NaCl,
故答案为:CH3CH2CH2CH2Cl+NaOH$→_{△}^{H_{2}O}$CH3CH2CH2CH2OH+NaCl;
(2)反应有大量热放出,1-氯丁烷溶液易挥发,反应装置中的长玻璃管除导气外,还对对挥发的反应物起冷凝回流作用.
故答案为:导气、冷凝回流;
(3)反应在碱性条件下水解,检验氯离子,应先加入硝酸酸化,避免生成AgOH沉淀而干扰实验,故答案为:免生成AgOH沉淀而干扰实验;
(4)用该装置,还可制备硝基苯,实验室制备乙烯需加热到170℃,乙酸乙酯不能水浴加热,制备溴苯不用加热,故答案为:A.
点评 本题有机物的制备以及性质实验的设计,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理、操作方法,难度不大.


科目:高中化学 来源: 题型:选择题
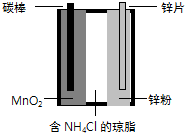 已知离子可在琼脂中移动.某简易电池如图所示.放电时,下列说法错误的是( )
已知离子可在琼脂中移动.某简易电池如图所示.放电时,下列说法错误的是( )| A. | 锌极上电极反应式为:Zn-2e-=Zn2+ | B. | MnO2得电子被还原 | ||
| C. | NH4+离子通过琼脂向锌极移动 | D. | 外电路电流的方向从碳棒到锌片 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
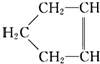 可简写为
可简写为 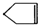 .降冰片烯的分子结构可表示为
.降冰片烯的分子结构可表示为
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | A | B |
| 研究目的 | 压强对反应的影响 | 温度对反应的影响 |
| 图示 |  | 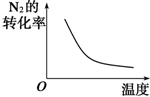 |
| 选项 | C | D |
| 研究目的 | 平衡体系中增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )
八角茴香属于草本植物,是我国民间常用做烹调的香料.医学研究成果显示,从八角茴香中可提取到莽草酸,莽草酸有抗炎、镇痛作用,也是合成对禽流感病毒有一定抑制作用的一种药物“达菲”的前体.莽草酸的结构式如图所示,下列关于莽草酸的说法正确的是( )| A. | 莽草酸的分子之间可能发生酯化反应 | |
| B. | 莽草酸的分子式为C7H4O5 | |
| C. | 莽草酸中含有苯环 | |
| D. | 莽草酸不能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质(杂质) | 试剂 | 有关离子方程式 |
| NaHCO3(Na2CO3) | ||
| FeCl2(FeCl3) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.69mol/L 14.5% | B. | 8.15mol/L 15.4% | C. | 7.69mol/L 15.4% | D. | 8.17mol/L 14.5% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com