
【题目】如图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和条件被略去。A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;B、C、E是常见气体,G的焰色反应呈黄色;I的溶液呈黄色。

请回答下列问题:
(1)写出下列物质的化学式A___、F___、X___;
(2)说出黄绿色气体C的一种用途____;
(3)实验室检验H中所含的金属阳离子的方法是:___;
(4)写出Y和D溶液反应的离子方程式___;
(5)写出I与X溶液反应的化学方程式___。
【答案】Na AlCl3 Fe 工业制盐酸、杀菌、消毒、农药生产、药物合成等 先加KSCN溶液(或硫氰化钾溶液)无明显现象,再加氯水,溶液变为血红色 ![]()
![]()
【解析】
金属单质Y既能与强酸反应,又能与强碱反应,应为Al,金属单质A与水反应生成D,D可与铝反应,且G的焰色反应呈黄色,可知D应含有Na元素,则A为Na,D为NaOH,B为H2,G为NaAlO2,气体C与氢气反应,且与铝反应,气体C应为Cl2,则F为AlCl3,E为HCl,由E→H→I的转化关系可知金属X为变价金属,应为Fe,则H为FeCl2,I为FeCl3。
(1)由以上分析可知A为Na,F为AlCl3,X为Fe;
故答案为:Na;AlCl3;Fe;
(2)C为氯气,可用于工业制盐酸或自来水的杀菌消毒或农药生产、药物合成等;
故答案为:工业制盐酸、杀菌、消毒、农药生产、药物合成等;
(3)H为FeCl2,检验亚铁离子的方法为:先加入KSCN溶液,没有现象,再加入氯水,如溶液变为血红色,说明含有亚铁离子;
故答案为:先加入KSCN溶液,没有现象,再加入氯水,如溶液变为血红色,说明含有亚铁离子;
(4)Y和D溶液反应的离子方程式为:![]() ;
;
故答案为:![]() ;
;
(5) I与X溶液反应的化学方程式为:![]() ;
;
故答案为:![]() ;
;


 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】请用下图所示仪器装置设计一个包括电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。其中A是金属Fe,B是石墨电极。
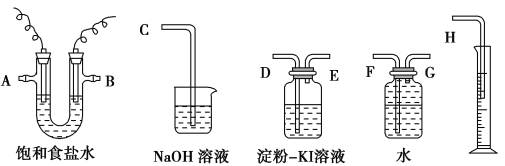
(1)所选仪器连接时,各接口的顺序是(填各接口的代号字母):A接______,________接______,B接________,________接________。
(2)实验时,装置中的石墨电极接电源的________极,所发生的电极反应式为_____________;铁电极接电源的________极,所发生的电极反应式为___________;
此电解总反应的离子方程式为________________________________。
(3)实验测得产生的氢气体积(已折算成标准状况)为5.60 mL,电解后溶液的体积恰好为50.0 mL,则溶液中OH—的浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、磷、硫等元素形成的单质和化合物在生活、生产中有重要的用途。
(1)下列氮原子的电子排布图表示的状态中,能量由低到高的顺序是___(填字母)。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(2)P4S3可用于制造火柴,其分子结构如图所示:
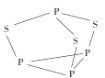
①P4S3分子中硫原子的杂化轨道类型为___。
②1molP4S3分子中含有的孤电子对的数目为___对。
(3)科学家合成了一种阳离子“N5n+”,其结构是对称的,5个N排成“V”形,每个N都达到8电子稳定结构,且含有2个氮氮三键,此后又合成了一种含有“N5n+”的化学式为“N8”的离子晶体(该晶体中每个N原子都达到了8电子稳定结构),N8的电子式为___。(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为___。
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为___。

(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和对应金属阳离子的半径。随着金属阳离子半径的增大,碳酸盐的热分解温度逐渐升高,原因是___。
碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 402 | 900 | 1172 | 1360 |
金属阳离子半径/pm | 66 | 99 | 112 | 135 |
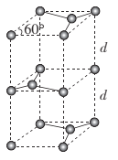
(6)石墨的晶胞结构如图所示。已知石墨的密度为ρg·cm-3,C-C键的键长为rcm,NA为阿伏加德罗常数的值,则石墨晶体的层间距d=___cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块镁铝合金(不含其它物质)投入到50ml的稀盐酸溶液中,充分反应后,固体无剩余,向所得溶液中逐滴滴入cmol/LNaOH溶液时,得到沉淀的质量与所滴加NaOH溶液的体积有如图关系:
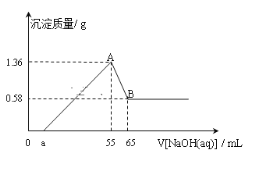
(1)图中B点表示沉淀的化学式为___;AB段发生反应的离子方程式为___。
(2)合金中金属铝的物质的量为___mol;
(3)稀盐酸溶液的浓度为___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Mg2+、NH4+、Al3+、Fe3+、CO32—、SO42—、Cl—中的几种。若加入锌粒,产生无色无味的气体;若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法不正确的是
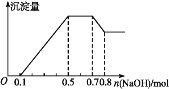
A. 溶液中的阳离子有H+、Mg2+、NH4+、Al3+
B. 溶液中n(Al3+)=0.1 mol
C. 溶液中一定不含CO32—,可能含有SO42—和Cl—
D. n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】流动电池可以在电池外部调节电解质溶液,从而维持电池内部电解质溶液浓度稳定,原理如图。下列说法错误的是
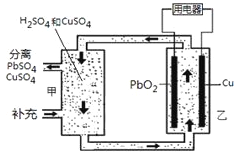
A.Cu为负极
B.PbO2电极的电极反应式为:PbO2+ 4H++ SO42-+ 2e-= PbSO4+ 2H2O
C.甲中应补充硫酸
D.当消耗1 mol PbO2,需分离出2 mol CuSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )
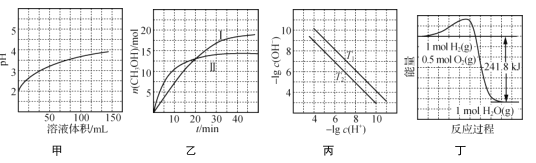
A. 图甲表示1 mL pH=2某一元酸溶液加水稀释时,pH随溶液总体积的变化曲线,说明该酸是强酸
B. 图乙表示恒容密闭容器中其他条件相同时改变温度,反应CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ
CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ
C. 图丙表示不同温度下水溶液中-lg c(H+)、-lg c(OH-)变化曲线,说明T1>T2
D. 图丁表示1 mol H2和0.5 mol O2反应生成1 mol H2O过程中的能量变化曲线,说明H2的燃烧热是241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组欲通过以下实验来探究Na2CO3和NaHCO3两种物质的性质。
(1)称取两种固体各2g,分别放入两个试管中,分别滴入几滴水,振荡,测量温度变化;继续向各试管中滴加10mL蒸馏水,用力振荡,待固体充分溶解,并恢复至室温后,向所得溶液中各滴入2滴酚酞试液。
① 发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得到结论____________。
② 同学们在两试管中还观察到了其它现象。其中,盛放Na2CO3的试管中出现的现象(填字母序号)_______________。
A.溶液温度下降 B.溶液温度升高 C.滴入酚酞后呈无色 D.滴入酚酞后呈红色
(2)如图所示。
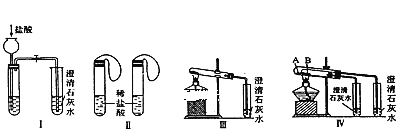
①若能用装置Ⅳ来验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是____;
②若用实验来鉴别碳酸钠和碳酸氢钠两种固体,上述装置能达到实验目的的是(填装置序号)_____;
③在气密性良好的装置II两个气球中分别放入1gNaHCO3和1gNa2CO3固体,将气球内的固体同时倒入盛有3mL 1 mol·L-1盐酸的试管中。反应结束后,气球均有膨胀,恢复至室温。下列说法正确的是__________。
A.装NaHCO3的气球体积较大 B.装Na2CO3的气球体积较大
C.生成气体的体积均根据盐酸计算 D.生成气体的体积均根据固体计算
④若采用装置Ⅲ测定Na2CO3固体中混有的少量NaHCO3的质量分数,其计算所需的数据有反应前固体样品的总质量和_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学中常用的物理量,请完成以下有关其计算的内容。
(1)0.2 g H2含有___________________个H原子。
(2)100 mL 某Al2(SO4)3溶液中,c(Al3+) = 2.0 mol/L,则其中c(SO42-) = _________mol/L。
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是________。
(4)当CO、CO2的分子个数之比为1:2时,原子总数之比为___________,质量之比为________;标准状况下,密度之比为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com