
����Ŀ������ѧһѡ��3:���ʽṹ�����ʡ������ꡢ���Ƚ������仯�����ڿ�ѧ�о���ҵ������Ӧ��ʮ�ֹ㷺���ش���������:
(1)��̬��ԭ�ӵļ۵����Ų�ʽΪ________�������ܡ����Ļ�̬ԭ�Ӻ���δ�ɶԵ��������ٵ���_____________
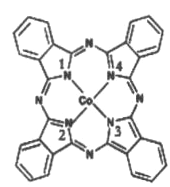
(2)̪ݼ�ܷ��ӵĽṹ��ʽ��ͼ��ʾ,��������Ϊ������,̪�ܷ�������������ͨ����λ����ϵĵ�ԭ�ӵı����__________ (��1��2��3��4)�����ַǽ���ԭ�ӵĵ縺���ɴ�С��˳��Ϊ____(����Ӧ��Ԫ�ط��ű�ʾ);̼ԭ�ӵ��ӻ��������Ϊ_________
(3)Fe(CO)x�����³�Һ̬,�۵�Ϊ-20.5��,�е�Ϊ103��,�����ڷǼ����ܼ�,�ݴ˿��ж�Fe(CO) x��������_______ (�������),�������Fe(CO) x������ԭ�Ӽ۵������������ṩ������֮��Ϊ18,��x=_________
(4)NiO��FeO�ľ���ṹ�������Ȼ��Ƶ���ͬ,Ni2+��Fe2+�����Ӱ뾶�ֱ�Ϊ69pm��78pm,���۵�NiO ______ FeO(�>����<����=��),ԭ����___________________________��
(5)NiAs�ľ����ṹ��ͼ��ʾ:
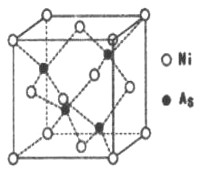
�������ӵ���λ��Ϊ_________��
���������ӵ�������ֵΪNA,�����ܶ�Ϊpg.cm-1,��þ��������������֮��ľ���Ϊ_____cm��(д���������ʽ)
���𰸡� 3d74s2 �� 2��4 N>C>H sp2 ���Ӿ��� 5 �� ��ͬ��ɵ����ӣ��뾶ԽС�����Ӽ�ľ���������Խ�����Ӿ���ľ�����Խ�� 4 ![]() ����536/NA��p cm
����536/NA��p cm
����������1��CoΪ27��Ԫ�أ�ԭ�Ӻ��������Ϊ27�������������ԭ�������������Ų�ʽΪ:![]() ����ԭ�ӵļ۵����Ų�ʽΪ3d74s2�������ܡ�����ԭ�Ӻ�������Ų�Ϊ3d64s2 ��3d74s2 ��3d84s2����˺���δ�ɶԵ��������ٵ���������ȷ�𰸣�3d74s2 ������
����ԭ�ӵļ۵����Ų�ʽΪ3d74s2�������ܡ�����ԭ�Ӻ�������Ų�Ϊ3d64s2 ��3d74s2 ��3d84s2����˺���δ�ɶԵ��������ٵ���������ȷ�𰸣�3d74s2 ������
��2����ͼ�п�֪��̪�ܷ�������������ͨ����λ����ϵĵ�ԭ�ӵı����2��4��̪ݼ�������ַǽ���ԭ��ΪC��N��H,ͬ����������ҵ縺������,�ǽ�����Խǿ�縺��Խ��,�ʵ縺��N>C>H ��������Cԭ�Ӿ��γ�3��![]() ��,û�й¶Ե���,�ӻ������ĿΪ3,̼ԭ�ӵ��ӻ��������Ϊ
��,û�й¶Ե���,�ӻ������ĿΪ3,̼ԭ�ӵ��ӻ��������Ϊ![]() ����ȷ�𰸣� 2��4 �� N>C>H�� sp2 ��
����ȷ�𰸣� 2��4 �� N>C>H�� sp2 ��
(3)���Ӿ�����۷е�ϵ������������Ϣ֪�������ʵ��۷е�ϵ�������Ϊ���Ӿ����������![]() ������ԭ������ԭ������۵�������8��ÿ�������ṩ�ĵ�������2��
������ԭ������ԭ������۵�������8��ÿ�������ṩ�ĵ�������2��![]() ��
��![]() ����ȷ�𰸣����Ӿ��壻5 ��
����ȷ�𰸣����Ӿ��壻5 ��
��4��![]() ��
��![]() �ľ���ṹ���;����Ȼ��Ƶ���ͬ,˵�����߶������Ӿ��������Ӿ�����۵������Ӽ���ǿ���й��� ��ͬ��ɵ����ӣ��뾶ԽС�����Ӽ�ľ���������Խ�����Ӿ���ľ�����Խ���۵�Խ�ߣ� ��Ϊ
�ľ���ṹ���;����Ȼ��Ƶ���ͬ,˵�����߶������Ӿ��������Ӿ�����۵������Ӽ���ǿ���й��� ��ͬ��ɵ����ӣ��뾶ԽС�����Ӽ�ľ���������Խ�����Ӿ���ľ�����Խ���۵�Խ�ߣ� ��Ϊ![]() �����Ӱ뾶С��
�����Ӱ뾶С��![]() �����Ӱ뾶�������۵���
�����Ӱ뾶�������۵���![]() ����ȷ�𰸣�����ͬ��ɵ����ӣ��뾶ԽС�����Ӽ�ľ���������Խ�����Ӿ���ľ�����Խ���۵�Խ�ߡ�
����ȷ�𰸣�����ͬ��ɵ����ӣ��뾶ԽС�����Ӽ�ľ���������Խ�����Ӿ���ľ�����Խ���۵�Խ�ߡ�
��5����������ԭ����ĿΪ![]() ����ԭ����ĿΪ4������������Ϊ4����59+75��/NAg, �������=4����59+75��/NA��p=536/ NA��pcm3�����ⳤr=
����ԭ����ĿΪ4������������Ϊ4����59+75��/NAg, �������=4����59+75��/NA��p=536/ NA��pcm3�����ⳤr= ![]() ����ԭ������Χ��4����ԭ���γ���������ṹ����ԭ�����������嶥�����ľ����������ԭ������ԭ�����ߴ��ھ�����Խ���������Ϊ��Խ��߳��ȵ�
����ԭ������Χ��4����ԭ���γ���������ṹ����ԭ�����������嶥�����ľ����������ԭ������ԭ�����ߴ��ھ�����Խ���������Ϊ��Խ��߳��ȵ�![]() �����ھ����ⳤ��
�����ھ����ⳤ��![]() r�����������������Ϊ
r�����������������Ϊ![]() ��
��![]() ;��ȷ�𰸣�
;��ȷ�𰸣� ![]() ��
��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ϼ�G�����������кܶ���;,��ϳ�·������:

��֪:��R1��CHO+R2��CH2��CHO![]()
![]() (R1��R2������������ԭ��)
(R1��R2������������ԭ��)
��D��A��Ϊͬϵ��;����ͬ������,D����������������ܶ�Ϊ39��
(1)A��������____,G�к��������ŵ�������____��
(2)�ڵķ�Ӧ������____,B��F�Ľṹ��ʽ�ֱ�Ϊ______��______��
(3)д��һ���ܼ���A��D���Լ�:______;C�ж���ͬ���칹��,�������ڷ����廯�������____�֡�
(4)д����Ӧ�ٵĻ�ѧ����ʽ:_____________��
(5)G��ͬ���칹�� ��һ����Ҫ��ҩ���м���,��ϳ�·����G����,����
��һ����Ҫ��ҩ���м���,��ϳ�·����G����,����![]() Ϊԭ��������ĺϳ�·��(��������ԭ����ѡ)_________��
Ϊԭ��������ĺϳ�·��(��������ԭ����ѡ)_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ָ����(C5H8)nͨʽ�������Լ��䲻ͬ���ͳ̶Ⱥͺ�����������,�㷺�����ڶ�ֲ�����ڡ��������л���a��b�����������,�й����ǵ�˵������ȷ����
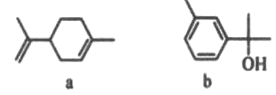
A. b�ķ���ʽΪC10H14O
B. a����Ԫ���ϵ�һ�ȴ��ﹲ��5��(�����������칹)
C. a��b����������̼ԭ�Ӿ�����ͬһƽ����
D. ��������ˮ������a��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2SO2(g)��O2(g)![]() 2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1 mol SO2(g)����Ϊ1 mol SO3(g)����H����99 kJ��mol��1����ش��������⣺
2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1 mol SO2(g)����Ϊ1 mol SO3(g)����H����99 kJ��mol��1����ش��������⣺
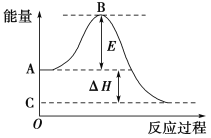
��1��ͼ��A���ʾ��___________, B���ʾ��__________��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ��________(����������������)Ӱ�졣
��2��ͼ����H��________kJ��mol��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������X����������������ͭ��ɣ�ȡ������ȵ�������������ͼ��ʾ����ʵ�飺 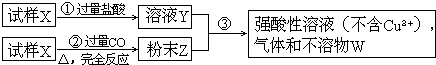
��1����д�����������������ȫ����Ӧ�����ӷ���ʽ��
��2����ȫ������ҺY��ȫ���ķ�ĩZ��ַ�Ӧ�����ɵIJ�����W��������m����ÿ������X������ͭ������Ϊ �� ����m��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪1mol������������ȫȼ������ˮ�����ų�241.8ǧ�������������Ȼ�ѧ����ʽ��ȷ����
A. 2H2��g��+O2��g����2H2O��g��+241.8kJ
B. H2��g��+1/2O2��g����H2O��s��+241.8 kJ
C. H2��g��+1/2O2��g����H2O��g��-241.8 kJ
D. H2O��g����H2��g��+1/2O2��g��-241.8 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������dz��������ֽ��������ǵĵ��ʼ������������������д����ɼ���
��1������������ϡ���ᷢ����Ӧ��������Fe(NO3)2��NO��д���÷�Ӧ�Ļ�ѧ����ʽ___________��
��2��ʵ��������FeSO4��Һʱ�����û�и���������FeSO4�ᱻ����Ϊ_______����д��ѧʽ�����ڸ���Һ�м���___________�Լ�������_____________________����֤����Һ���ʡ�
��3��KAl(SO4)2��12H2O�׳���������������ˮ����������ԭ��д���йص����ӷ���ʽ____________________��
��4����֪Ba(AlO2)2������ˮ����ͼ��ʾ������Al2(SO4)3��Һ����μ���Ba(OH)2��Һʱ�����ɳ��������ʵ���y�����Ba(OH)2�����ʵ���x�Ĺ�ϵ��
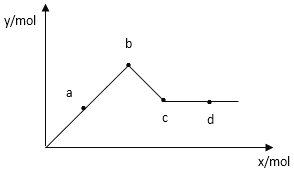
��ͼ��֪c��ij�����________���ѧʽ������֪a-bʱ���ڵij�����Al(OH)3��BaSO4�����ߵ����ʵ���:________��________�ࡣ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���п��淴ӦFe��s��+CO2��g��FeO��s��+CO��g������֪���¶�938Kʱ��ƽ�ⳣ��K=1.5����1173Kʱ��K=2.2������������ȷ���ǣ�������
A.�÷�Ӧ�ﵽƽ��״̬ʱc��CO2��=c��CO��
B.�÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ
C.����ʼʱ��Fe��2.0mol CO2��������̶�Ϊ1 L���ܱ������У�ij�¶�ʱ�ﵽƽ�⣬��ʱ������CO��Ũ��Ϊ1.0 mol/L������¶���������Ӧ��ƽ�ⳣ��K=1.0
D.���÷�Ӧ������̶����ܱ������н��У��ں����´ﵽƽ��״̬����ͨ��CO��Ӧ���������CO2�����ʵ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���Թ�ҵ��ˮ�к���K2Cr2O7 �� �����£����ᣨH2C2O4���ܽ����е�Cr2O72��ת��ΪCr3+ �� ij�������о����֣�����������[Al2Fe��SO4��424H2O]���ɶԸ÷�Ӧ������ã�Ϊ��һ���о��й����ضԸ÷�Ӧ���ʵ�Ӱ�죬̽�����£�
��1����25���£����ƹ���ǿ�ȡ���ˮ��Ʒ��ʼŨ�Ⱥʹ���������ͬ�����ڲ�ͬ�ij�ʼpH��һ��Ũ�Ȳ�����Һ���������Ա�ʵ�飬�������ʵ����Ʊ�
ʵ���� | ��ʼpH | ��ˮ��Ʒ���/mL | ������Һ���/mL | ����ˮ���/mL |
�� | 4 | 60 | 10 | 30 |
�� | 5 | 60 | 10 | 30 |
�� | 5 | 60 |
���ʵ��ٺ͢���Һ�е�Cr2O72��Ũ����ʱ��仯��ϵ��ͼ��ʾ��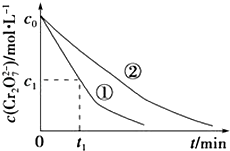
��2��������Ӧ����ᱻ���������ӷ���ʽΪ
��3��ʵ��ٺ͢ڵĽ��������ʵ�����0��t1ʱ��η�Ӧ����v��Cr3+��=molL��1min��1���ô���ʽ��ʾ����
��4���ÿ������������[Al2Fe��SO4��424H2O]��������õijɷ�������¼��裬������ɼ�����ͼ������� ����һ��Fe2+������ã�
���������
����������
��5���������ʵ����֤��������һ������±������ݣ� ����������ʵ���ṩ���Լ��⣬�ɹ�ѡ���ҩƷ��K2SO4��FeSO4��K2SO4Al2��SO4��324H2O��Al2��SO4��3�ȣ���Һ��Cr2O72����Ũ�ȿ��������ⶨ��
ʵ�鷽������Ҫ��д����������̣� | Ԥ��ʵ�����ͽ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com