
����Ŀ����֪��
CH3CH2CH2CH3��g��+ ![]() O2��g���T4CO2��g��+5H2O��l����H=��2 878kJ/mol
O2��g���T4CO2��g��+5H2O��l����H=��2 878kJ/mol
��CH3��2CHCH3��g��+ ![]() O2��g���T4CO2��g��+5H2O��l����H=��2 869kJ/mol
O2��g���T4CO2��g��+5H2O��l����H=��2 869kJ/mol
����˵����ȷ���ǣ� ��
A.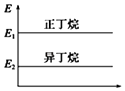
���������춡���������С��ϵ��ͼ
B.��������ȶ��Դ����춡��
C.�춡��ת��Ϊ������Ĺ�����һ�����ȹ���
D.�춡������е�̼�����������Ķ�
���𰸡�A
���������⣺�������Ϣ��֪CH3CH2CH2CH3��g��=��CH3��2CHCH3��g����H=��9KJ/mol��
A����������ӵ����������춡�������������������춡���������С��ϵ��ͼ����A��ȷ��
B������Խ��Խ���ȶ��������鲻�ȶ�����B����
C����������ӵ����������춡�����������춡��ת��Ϊ������Ĺ�����һ�����ȹ��̣���C����
D����������춡�����ʽ��ͬ��������ͬ��C��H������D����
��ѡA��
�����㾫����������Ҫ�����˷�Ӧ�Ⱥ��ʱ�����֪ʶ�㣬��Ҫ�����ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�Ȳ�����ȷ�����⣮


 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д� Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£������pH����ͬ��������Ȼ����Һ��ˮϡ��ʱ��pH�仯������ͼ��ʾ�������ж���ȷ���ǣ� �� 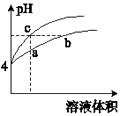
A.a��c������Һ�ĵ���������ͬ
B.a��b��c������Һ��ˮ�ĵ���̶ȣ�a��b��c
C.b����Һ�У�c��H+��+c��NH3H2O��=c��OH����
D.��NaOH��Һ�͵����b��c����Һ��Ӧ������NaOH��Һ�����Vb=Vc
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5 �� ��ӦPCl5��g��=PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 50 | 150 | 250 | 350 |
n��PCl3��/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
����˵����ȷ���ǣ� ��
A.��Ӧ��ǰ50 s ��ƽ������v��PCl3��=0.0032 molL��1s��1
B.���������������䣬�����¶ȣ�ƽ��ʱc��PCl3��=0.11 molL��1 �� ��Ӧ�ġ�H��0
C.��ͬ�¶��£���ʼʱ�������г���1.0 mol PCl5��0.20 mol PCl3 ��0.20 mol Cl2 �� ��Ӧ�ﵽƽ��ǰv��������v���棩
D.��ͬ�¶��£���ʼʱ�������г���2.0 mol PCl3 ��2.0 mol Cl2 �� �ﵽƽ��ʱ��PCl3 ��ת����С��80%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��������ij��������Ʒ���Ƿ����������ƣ���Ʒ������£�ȡ�������������Һ������Һ�еμ���������KMnO4��Һ���۲���Һ�Ƿ���ɫ�������Һ��ɫ��ȥ��˵������Ʒ�к����������ƣ� 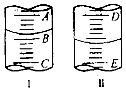
��1�������ӷ���ʽ��ʾ�÷�Ӧԭ���� ��
��2��ͼI��ʾ100mL��Ͳ��Һ���λ�ã�A��B��B��C�̶ȼ����10mL������̶�AΪ30����Ͳ��Һ��������mL��ͼII��ʾ25mL�ζ�����Һ���λ�ã����Һ�洦�Ķ�����a����ζ�����Һ������������ĸ��
A������amL B�����ڣ�25��a��mL C������amL D�����ڣ�25��a��mL
��3����С��ͬѧ���ⶨ��Ʒ���������Ƶĺ����������������£�
a����ȡmg��Ʒ��������ˮ�ܽⲢ������ƿ��
b����V1mL C1mol/L������KMnO4��Һ��������������ƿ����
c����C2mol/L�����ƣ�Na2C2O4����Һ�ζ�������KMnO4 �� ���ζ��յ�ʱ��ȥNa2C2O4��ҺV2mL
��KMnO4��ҺӦװ��ʽ�ζ����У��ﵽ�ζ��յ�ʱ��Һ��ɫ�ı仯 ��
����Ʒ��Na2SO3�����ʵ���Ϊmol�����ú�C1��V1��C2��V2�Ĵ���ʽ��ʾ����
��4�����в����ᵼ�²�õ�Na2SO3�����ʵ���ƫ�ߵ���������ĸ��˫ѡ����
A.δ��Na2C2O4��Һ��ϴ�ζ���
B.�ζ�ǰ����ʢ��Na2C2O4��Һ�ĵζ��ܣ��ζ�����
C.�ζ�ǰ�ζ��ܼ��촦�����ݣ��ζ�����ʧ
D.�ζ�ʱҡ����ƿ��ƿ�е�Һ�ν�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤����������ֵ����ش��������⣺
��1��0.5mol SO2������Լ��ԭ�ӣ�����g SO3������ԭ������ȣ�
��2��������ͬ�Ģ�HCl����NH3����CO2����O2���������У���ͬ��ͬѹ�����£���ռ�����С���ǣ�����ţ� ��
��3��19gij���۽����Ȼ��ACl2���к���0.4mol Cl�� �� ��ACl2��Ħ����������
��4����״����ij��O2��N2�Ļ������m g������b�����ӣ���n g�û����������ͬ״������ռ�����Ӧ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������������һ����̼�������з�Ӧ��Fe2O3��s��+3CO��g��2Fe��s��+3CO2��g��
��1���ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ��K= ��
�ڸ��¶��£���2Lʢ��Fe2O3��ĩ���ܱ�������ͨ��CO���壬10min�������˵�����11.2g����10min��CO��ƽ����Ӧ��Ϊ ��
��2��˵���÷�Ӧ�Ѵﵽƽ��״̬�� ��
a��CO��CO2������������������������ȣ�
b��CO����CO2�����������ٸı�
c��CO����CO2�����������50%
��3��I2O5��ʹH2S��CO��HCl�������������ڶ����ⶨCO�ĺ�������֪��
2I2��s��+5O2��g��=2I2O5��s����H1=��75.56kJmol��1
2CO��g��+O2��g��=2CO2��g����H2=��566.0kJmol��1
д��CO��g����I2O5��s����Ӧ����I2��s����CO2��g�����Ȼ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˽�����Na2SO4��NaHCO3��NaCl�����ᴿ���Ƶô������Ȼ�����Һ��ijѧ���������ͼ��ʾ��ʵ�鷽����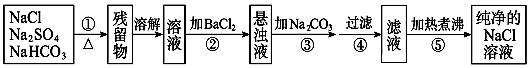
��֪̼�������ڼ����������ֽܷ��̼���ơ�������̼��ˮ����NaCl��Na2SO4�������ʱ��������ѧ�仯����ش��������⣺
��1��������ʢ��ҩƷ��ѡ�������������ƣ���
��2��������Ϊʲô����Ba��NO3��2��Һ���������ǣ� ��
��3�����в����ں��ж�SO42���ѳ����ķ����ǣ� ��
��4�������۵�Ŀ���ǣ� ��
��5������Ʒ����Ƿ���������ǡ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.126C��146C��2�ֺ��أ����ǻ���ͬλ��
B.���ڻ�ѧ�о��߿���������Ϊ������̬�Ĺ���̼�������µ�̼�ṹ������������ĭ�������������ƺ��࣬���ؼ�С�������д��ԣ�������ĭ̼��C60����ͬ��������
C.![]() ��
��  ��Ϊͬ���칹��
��Ϊͬ���칹��
D.�������ɿ������� ![]() �ͩ�NO2���ֻ������
�ͩ�NO2���ֻ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ȥ�����е�CaCl2��MgCl2��Na2SO4 �Լ���ɳ�����ʣ�ijͬѧ�����һ���Ʊ����ε�ʵ�鷽�����������£�![]()
��1���ж�BaCl2�ѹ����ķ�������
��2���ڢ��У���ص����ӷ���ʽ����
��3��Ϊ���龫�δ��ȣ�������230mL0.2mol/L NaCl(����)��Һ��������������ƽ��ȡ���ι��������Ϊ �� ��Ҫ�IJ�����������Ͳ�� ��
��4������NaCl(����)��Һʱ�����������в�������ɽ��ƫ�͵�����
A������ʱNaCl�ѳ��� B����ƽ����������ʴ
C������ҡ��ʱ��Һ���½��ּ�ˮ D������ʱ���ӿ̶���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com