
 氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答:
氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答:分析 (1)氯碱工业生产氯气,电解饱和食盐水;
(2)用氯气与烧碱溶液反应制备84消毒液,生成NaCl、NaClO、水;
(3)用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯,还生成NaCl;
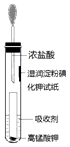
(4)①碱性溶液及具有还原性的物质可吸收氯气;
②说明Cl2的氧化性强于I2的实验,利用氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性说明.
解答 解:(1)氯碱工业生产氯气,电解饱和食盐水,反应为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑,故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑;
(2)用氯气与烧碱溶液反应制备84消毒液,生成NaCl、NaClO、水,离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯,还生成NaCl,反应为Cl2+2NaClO2=2ClO2+2NaCl,故答案为:Cl2+2NaClO2=2ClO2+2NaCl;
(4)①C为碱性溶液,B具有还原性,则BC中的物质可吸收氯气,故答案为:BC;
②说明Cl2的氧化性强于I2的实验,氯气氧化KI生成碘,使淀粉KI试纸变蓝,即湿润淀粉碘化钾试纸变蓝能说明Cl2的氧化性强于I2,由于同主族元素从上到下,原子半径依次变大,得电子能力依次减弱,氧化能力依次减弱,故答案为:湿润淀粉碘化钾试纸变蓝;同主族元素从上到下,原子半径依次变大,得电子能力依次减弱,氧化能力依次减弱.
点评 本题考查氯气的化学性质,为高频考点,把握习题中的信息、物质的氧化性及发生的反应为解答的关键,侧重分析能力与化学用语应用的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 催化还原CO2是解决温室效应及能源问题的重要手段之一.研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO.反应的热化学方程式如下:
催化还原CO2是解决温室效应及能源问题的重要手段之一.研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO.反应的热化学方程式如下:| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
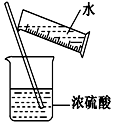 进行化学实验必须注意安全,下列说法中正确的组合是( )
进行化学实验必须注意安全,下列说法中正确的组合是( )| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(K) CO2转化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | c(NO)/mol•L-1 | c(CO)/mol•L-1 |
| 0 | 1.00×10-3 | 3.60×10-3 |
| 1 | 4.50×10-4 | 3.05×10-3 |
| 2 | 2.50×10-4 | 2.85×10-3 |
| 3 | 1.50×10-4 | 2.75×10-3 |
| 4 | 1.00×10-4 | 2.70×10-3 |
| 5 | 1.00×10-4 | 2.70×10-3 |
| 化学式 | 电离常数 |
| H2SO3 | K1=1.3×10-2,K2=6.2×10-8 |
| H2CO3 | K1=4.3×10-7,K2=5.6×1011 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com