
ЁОЬтФПЁПдзгНсЙЙгыаджЪ
ЃЈ1ЃЉдЊЫиAsгыNЭЌзхЁЃAsЕФЧтЛЏЮяЗаЕуБШNH3ЕФ___(ЬюЁАИпЁБЛђЁАЕЭЁБ)ЃЌЦфХаЖЯРэгЩЪЧ______ЁЃ
ЃЈ2ЃЉЭдзгдкЛљЬЌЪБЕФМлЕчзгХХВМЪНЮЊ______ЁЃ
ЃЈ3ЃЉFeЪЧШЫЬхашвЊВЙГфЕФдЊЫижЎвЛЃЌЪдаДГіFe2ЃЋЕФКЫЭтЕчзгХХВМЪНЃК_____ЁЃгыAlЭЌвЛжмЦкЕФNaЁЂMgдЊЫивВЪЧШЫЬхЫљашдЊЫиЃЌNaЁЂMgЁЂAlЛљЬЌдзгЕквЛЕчРыФмЕФДѓаЁЙиЯЕ____ЁЃФГЭЌбЇЫљЛЛљЬЌУОдзгЕФКЫЭтЕчзгХХВМЭМШчЭМ![]() ЃЌИУЭЌбЇЫљЛЕФЕчзгХХВМЭМЮЅБГСЫ______ЁЃ
ЃЌИУЭЌбЇЫљЛЕФЕчзгХХВМЭМЮЅБГСЫ______ЁЃ
ЃЈ4ЃЉKдЊЫиДІгкдЊЫижмЦкБэЕФ____ЧјЃЌЦфЛљЬЌдзгжаЃЌКЫЭтЕчзгеМОнЕФЕчзгдЦТжРЊЭМЮЊЧђаЮЕФФмМЖга____ИіЁЃ
ЁОД№АИЁПЕЭ АБЦјЗжзгжЎМфДцдкЧтМќЃЌAsH3ЗжзгМфЮЊЗЖЕТЛЊСІ 3d104s1 1s22s22p63s23p63d6 NaЃМAlЃМMg ФмСПзюЕЭдРэ s 4
ЁОНтЮіЁП
(1)АБЦјЗжзгжЎМфДцдкЧтМќЃЌAsH3ЗжзгМфЮЊЗЖЕТЛЊСІЃЌЧтМќБШНЯЗЖЕТЛЊСІИќЧПЃЛ
(2)КЫЭтЕчзгХХВМЪНЕФЪщаДвЊзЂвтКщЬиЙцдђЕФЬиР§ЁЃCuЪЧ29КХдЊЫиЃЛ
(3)ЬњдЊЫиЮЊ26КХдЊЫиЃЌЪЇШЅ2ЕчзгКѓаЮГЩFe2+ЃЛЭЌвЛжмЦкдЊЫиЕквЛЕчРыФмЫцзХдзгађЪ§діДѓЖјГЪдіДѓЧїЪЦЃЌЕЋЕкIIAзхЁЂЕкVAзхдЊЫиЕквЛЕчРыФмДѓгкЦфЯрСкдЊЫиЃЌNaЁЂMgЁЂAlЪєгкЭЌвЛжмЦкдЊЫиЃЛЕчзггІгХЯШХХСадк3sФмМЖЃЛ
(4)KдЊЫиДІгкдЊЫижмЦкБэЕФsЧјЃЌЦфЛљЬЌдзгжаЃЌКЫЭтЕчзгеМОнЕФЕчзгдЦТжРЊЭМЮЊЧђаЮЕФФмМЖЮЊnsФмМЖЁЃ
(1)АБЦјЗжзгжЎМфДцдкЧтМќЃЌAsH3ЗжзгМфЮЊЗЖЕТЛЊСІЃЌЧтМќБШНЯЗЖЕТЛЊСІИќЧПЃЌЙЪAsH3ЕФЗаЕуБШНЯNH3ЕФЕЭЃЛ
(2)CuЪЧ29КХдЊЫиЃЌКЫЭтЕчзгХХВМЪБЛЙвЊзёбКщЬиЙцдђЕФЬиР§ЃЌЙЪМлЕчзгХХВМЪНЪЧ3d104s1ЃЛ
(3)ЬњдЊЫиЮЊ26КХдЊЫиЃЌЦфКЫЭтЕчзгХХВМЮЊ1s22s22p63s23p63d64s2ЃЌЪЇШЅ2ЕчзгКѓаЮГЩFe2+ЃЌЙЪFe2+ЕФКЫЭтЕчзгХХВМЮЊЃК1s22s22p63s23p63d6ЃЛЭЌвЛжмЦкдЊЫиЕквЛЕчРыФмЫцзХдзгађЪ§діДѓЖјГЪдіДѓЧїЪЦЃЌЕЋЕкIIAзхЁЂЕкVAзхдЊЫиЕквЛЕчРыФмДѓгкЦфЯрСкдЊЫиЃЌЙЪNaЁЂMgЁЂAlЛљЬЌдзгЕквЛЕчРыФмЕФДѓаЁЙиЯЕЪЧNaЃМAlЃМMgЃЛЕчзггІгХЯШХХСадк3sФмМЖЃЌЮЅЗДСЫФмСПзюЕЭдРэЃЛ
(4)KдЊЫиДІгкдЊЫижмЦкБэЕФsЧјЃЌЦфЛљЬЌдзгжаЃЌКЫЭтЕчзгеМОнЕФЕчзгдЦТжРЊЭМЮЊЧђаЮЕФФмМЖЮЊnsФмМЖЃЌЗжБ№ЪЧ1sЁЂ2sЁЂ3sЁЂ4sЃЌМДКЫЭтЕчзгеМОнЕФЕчзгдЦТжРЊЭМЮЊЧђаЮЕФФмМЖга4ИіЁЃ


 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪЕбщНсТлгыЪЕбщВйзїМАЯжЯѓВЛЯрЗћЕФвЛзщЪЧЃЈ ЃЉ
бЁЯю | ЪЕбщВйзїМАЯжЯѓ | ЪЕбщНсТл |
A | ЯђФГЫсгъбљЦЗжаМгШыBa(OH)2ШмвКЃЌгаАзЩЋГСЕэЩњГЩ | ЫсгъЪдбљжавЛЖЈКЌSO42- |
B | ЯђKI-ЕэЗлШмвКжаЕЮШыТШЫЎЃЌШмвКБфГЩРЖЩЋ | I-ЕФЛЙдадЧПгкCl- |
C | НЋBa(OH)2ЁЄ8H2OКЭNH4ClОЇЬхдкаЁЩеБжаЛьКЯНСАшЃЌгУЪжДЅУўЩеБЭтБкИаОѕБфСЙ | Ba(OH)2ЁЄ8H2OгыNH4ClЕФЗДгІЪЧЮќШШЗДгІ |
D | ЯђФГбЮШмвКжаМгШыNaOHШмвКЃЌМгШШЃЌгУЪЊШѓЕФКьЩЋЪЏШяЪджНЗХдкЪдЙмПкЃЌЪджНБфРЖ | ИУбЮШмвКжаКЌгаNH4+ |
A.AB.BC.CD.D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. ЧтбѕШМСЯЕчГиЗХЕчЪБЛЏбЇФмШЋВПзЊЛЏЮЊЕчФм
B. ЗДгІ4Fe(s)+3O2(g)![]() 2Fe2O3(s)ГЃЮТЯТПЩздЗЂНјааЃЌИУЗДгІЮЊЮќШШЗДгІ
2Fe2O3(s)ГЃЮТЯТПЩздЗЂНјааЃЌИУЗДгІЮЊЮќШШЗДгІ
C. 3 mol H2гы1 mol N2ЛьКЯЗДгІЩњГЩNH3ЃЌзЊвЦЕчзгЕФЪ§ФПаЁгк6ЁС6.02ЁС1023
D. дкУИДпЛЏЕэЗлЫЎНтЗДгІжаЃЌЮТЖШдНИпЕэЗлЫЎНтЫйТЪдНПь
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСагаЙиЕчНтжЪШмвКЕФЫЕЗЈе§ШЗЕФЪЧ
A. Яђ0.1mol/LCH3COOHШмвКжаМгШыЩйСПЫЎЃЌШмвКжаc(H+)/c(CH3COOH)МѕаЁ
B. НЋCH3COONaШмвКДг20ЁцЩ§ЮТжС30ЁцЃЌШмвКжаc(CH3COO-)/c(CH3COOH)ЁЄc(OHЃ)діДѓ
C. ЯђбЮЫсжаМгШыАБЫЎжСжаадЃЌШмвКжаc(NH4+)/c(ClЃ)ЃО1
D. ЯђAgClЁЂAgBrЕФБЅКЭШмвКжаМгШыЩйСПЯѕЫсвјЃЌШмвКжаc(ClЃ)/c(BrЃ)ВЛБф
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПОпгаПЙОњзїгУЕФАзЭЗЮЬЫибмЩњЮяHЕФКЯГЩТЗЯпШчЯТЭМЫљЪОЃК
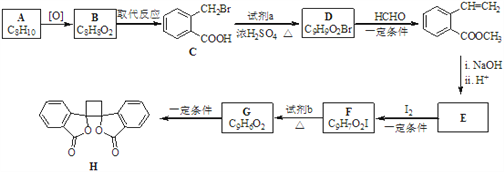
вбжЊЃКi.RCH2Br ![]() RЉHCЈTCHЉRЁф
RЉHCЈTCHЉRЁф
iiЃЎRЉHCЈTCHЉRЁф![]()
![]()
iiiЃЎRЉHCЈTCHЉRЁф![]()
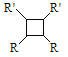
(вдЩЯRЁЂR'ЁЂR'ДњБэЧтЁЂЭщЛљЛђЗМЛљЕШ)
(1)AЪєгкЗМЯуЬўЃЌЦфУћГЦЪЧ_______________________ЁЃ
(2)DЕФНсЙЙМђЪНЪЧ_______________________________ЁЃ
(3)гЩFЩњГЩGЕФЗДгІРраЭЪЧ________________________________________ЁЃ
(4)гЩEгыI2дквЛЖЈЬѕМўЯТЗДгІЩњГЩFЕФЛЏбЇЗНГЬЪНЪЧ_____________________ЃЛДЫЗДгІЭЌЪБЩњГЩСэЭтвЛИігаЛњИБВњЮяЧвгыFЛЅЮЊЭЌЗжвьЙЙЬхЃЌДЫгаЛњИБВњЮяЕФНсЙЙМђЪНЪЧ_______________________________ЁЃ
(5)ЯТСаЫЕЗЈе§ШЗЕФЪЧ___________(бЁЬюзжФИађКХ)ЁЃ
A. GДцдкЫГЗДвьЙЙЬх
B. гЩGЩњГЩHЕФЗДгІЪЧМгГЩЗДгІ
C. 1 mol GзюЖрПЩвдгы1 mol H2ЗЂЩњМгГЩЗДгІ
D. 1 mol FЛђ1 mol HгызуСПNaOHШмвКЗДгІЃЌОљЯћКФ2 molNaOH
(6)вдввЯЉЮЊЦ№ЪМдСЯЃЌНсКЯвбжЊаХЯЂбЁгУБивЊЕФЮоЛњЪдМСКЯГЩ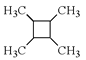 аДГіКЯГЩТЗЯп(гУНсЙЙМђЪНБэЪОгаЛњЮяЃЌгУМ§ЭЗБэЪОзЊЛЏЙиЯЕЃЌМ§ЭЗЩЯзЂУїЪдМСКЭЗДгІЬѕМў)ЁЃ___________________
аДГіКЯГЩТЗЯп(гУНсЙЙМђЪНБэЪОгаЛњЮяЃЌгУМ§ЭЗБэЪОзЊЛЏЙиЯЕЃЌМ§ЭЗЩЯзЂУїЪдМСКЭЗДгІЬѕМў)ЁЃ___________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЮТЖШЯТЃЌдквЛИі2 LЕФУмБеШнЦїжаЃЌМгШы4 mol AКЭ2 mol BНјааШчЯТЗДгІ3A(g)ЃЋ2B(g) ![]() 4C(s)ЃЋ2D(g)ЃЌЗДгІвЛЖЮЪБМфКѓДяЕНЦНКтЃЌВтЕУЩњГЩ1.6 mol CЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
4C(s)ЃЋ2D(g)ЃЌЗДгІвЛЖЮЪБМфКѓДяЕНЦНКтЃЌВтЕУЩњГЩ1.6 mol CЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
A. ИУЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЪЧ![]()
B. ДЫЪБЃЌBЕФЦНКтзЊЛЏТЪЪЧ40%
C. діДѓИУЬхЯЕЕФбЙЧПЃЌЛЏбЇЦНКтГЃЪ§діДѓ
D. діМгBЃЌBЕФЦНКтзЊЛЏТЪдіДѓ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаИїзщЮяжЪдкЪЪвЫЕФЬѕМўЯТЗДгІЃЌЦфжабѕЛЏМСгыЛЙдМСЕФЮяжЪЕФСПжЎБШЮЊ2ЃК1ЕФЪЧЃЈ ЃЉ
A. ![]()
B. Fe2O3+2Al![]() Al2O3+2Fe
Al2O3+2Fe
C. CaH2+2H2O===CaЃЈOHЃЉ2+2H2Ёќ
D. 3NO2+H2O===2HNO3+NO
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩшNaЮЊАЂЗќМгЕТТоГЃЪ§ЕФжЕЁЃвбжЊЗДгІЃК
ЂйCH4 (g) +2O2 (g) = CO2 (g) +2H2O(l) ЁїH1 =a kJ mol -1
ЂкCH4(g) + 2O2 (g) = CO2 (g) +2H2O(g) ЁїH2 =bkJ mol-1
МќФмЖЈвхЃКдкБъзМзДПіЯТЃЌНЋ1 molЦјЬЌЗжзгAB(g)НтРыЮЊЦјЬЌдзг
A(g)ЁЂB(g)ЫљашЕФФмСПЁЃвбжЊ1 molбѕЦјЕФМќФмЮЊxkJЁЃЦфЫћЪ§ОнШчЯТ БэЫљЪОЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЛЏбЇМќ | CЁЊO | CЁЊH | OЁЊH |
МќФм/(kJ mol-1) | 798 | 413 | 463 |
A.ЩЯЮФжаx=![]()
B.H2O(g) = H2O(1)ЕФЁїS<0ЁЂЁїH=(a ЁЊ b) kJ mol -1
C.ЕБга4NAИіOЁЊHМќЩњГЩЪБЃЌЗДгІЗХГіЕФШШСПЮЊa kJ
D.РћгУЗДгІЂйЩшМЦЕФдЕчГиЕчНтОЋСЖЭЃЌЕБИКМЋЪфГі0.2NAИіЕчзгЪБ. РэТлЩЯЕчНтВлЕФвѕМЋжЪСПдіжи6.4 g
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉввЯЉЪЙфхЫЎЭЪЩЋЕФЗДгІРраЭКЭЪЙЫсадИпУЬЫсМиШмвКЭЪЩЋЕФЗДгІРраЭ____(ЬюЁАЯрЭЌЁБЛђЁАВЛЯрЭЌЁБ)ЁЃ
ЃЈ2ЃЉгУБНжЦБИфхБНЕФЛЏбЇЗНГЬЪНЪЧ____ЃЌИУЗДгІЕФРраЭ___ЁЃ
ЃЈ3ЃЉвбжЊ2CH3CHOЃЋO2![]() 2CH3COOHЁЃШєвдввЯЉЮЊжївЊдСЯКЯГЩввЫсЃЌЦфКЯГЩТЗЯпШчЭМЫљЪОЁЃ
2CH3COOHЁЃШєвдввЯЉЮЊжївЊдСЯКЯГЩввЫсЃЌЦфКЯГЩТЗЯпШчЭМЫљЪОЁЃ
![]()
дђЗДгІЂкЕФЛЏбЇЗНГЬЪНЮЊ___ЃЌИУЗДгІЕФРраЭЮЊ___ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com