
| A. | 熔点-218℃,难溶于水 | |
| B. | 熔点3 900℃,硬度很大,不导电 | |
| C. | 难溶于水,固体时导电,升温时导电能力减弱 | |
| D. | 难溶于水,熔点高,固体不导电,熔化时导电 |
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有止血作用,特别对内脏的止血效果较好.
有止血作用,特别对内脏的止血效果较好. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①②③ | C. | ①②③⑤ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于50 mL | B. | 大于50 mL | C. | 等于100 mL | D. | 大于100 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
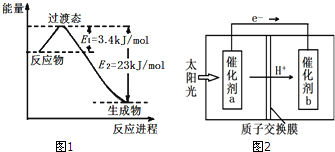 空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.
空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.| 温度(℃) | 300 | 500 | 700 |
| K | 3.00 | 3.47 | 4.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
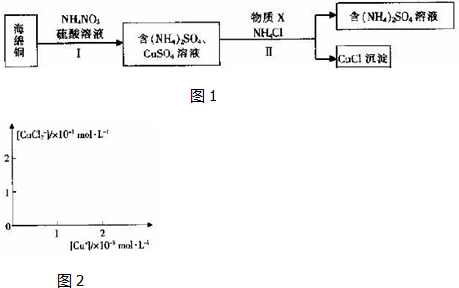
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 淀粉、纤维素、蛋白质在一定条件下均能发生水解反应,水解产物不相同 | |
| B. | 汽油、油脂不一定能使酸性高锰酸钾溶液褪色 | |
| C. | 煤的干馏、石油催化重整、石油裂化、煤的液化都属于化学变化 | |
| D. | 甘氨酸和谷氨酸在一定条件下最多能形成三种二肽 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com