
| A. | 取25.0gCuSO4•5H2O溶于1L水中 | |
| B. | 取16.0gCuSO4•5H2O溶于水,再稀释至1L | |
| C. | 将胆矾加热失去结晶水,再取无水硫酸铜16.0g溶于1L水 | |
| D. | 取25.0gCuSO4•5H2O溶于水,再稀释配成1L溶液 |
分析 A.硫酸铜晶体溶于1L水中,所得溶液体积不是1L;
B.16.0gCuSO4•5H2O的物质的量小于0.1mol;
C.硫酸铜溶于1L水,所得溶液的体积不是1L;
D.根据n=$\frac{m}{M}$计算出硫酸铜晶体的物质的量,再根据c=$\frac{n}{V}$计算出所得溶液浓度.
解答 解:A.25.0gCuSO4•5H2O的物质的量为0.1mol,0.1mol硫酸铜晶体溶于1L水中,所得溶液体积不是1L,溶液浓度不是0.1mol/L,故A错误;
B.取16.0gCuSO4•5H2O溶于水,再稀释至1L,溶液中硫酸铜的物质的量为:$\frac{16.0g}{250g/mol}$=$\frac{16}{25}$mol<0.1mol,则溶液浓度小于0.1mol/L,故B错误;
C.16.0g无水硫酸铜的物质的量为0.1mol,0.1mol硫酸铜溶于1L水,所得溶液浓度不是0.1mol/L,故C错误;
D.25.0gCuSO4•5H2O的物质的量为:$\frac{25.0g}{250g/mol}$=0.1mol,所得溶液浓度为:$\frac{0.1mol}{1L}$=0.1mol/L,故D正确;
故选D.
点评 本题考查了配制一定物质的量浓度的溶液的方法,题目难度不大,明确掌握配制一定物质的量浓度的溶液方法为解答关键,注意溶液体积与水的体积不同,为易错点,试题培养了学生的分析能力及化学实验、化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | SO3的水溶液能导电,所以SO3是电解质 | |
| B. | 自由移动离子数目多的电解质溶液导电能力一定强 | |
| C. | NaHSO4在水溶液里及熔融状态下均可电离出Na+、H+、SO${\;}_{4}^{2-}$ | |
| D. | NH3属于非电解质,但其水溶液能够导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| I1 | I2 | I3 | I4 | |
| 电离能(kJ•mol-1) | 578 | 1 817 | 2 745 | 11 578 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{r({K}^{+})}{r(K)}$ | B. | $\frac{r(Mg)}{r(Ca)}$ | C. | $\frac{r(Cl)}{r(C{l}^{-})}$ | D. | $\frac{r({S}^{2-})}{r({K}^{+})}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
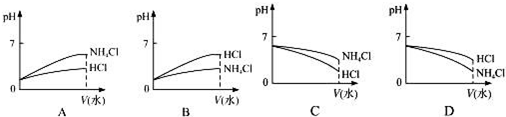
| 实验编号 | 氨水物质的量浓度/ (mol•L-1) | 盐酸物质的量浓度/ (mol•L-1) | 混合溶液pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲装置中电能转化为化学能 | B. | 乙装置中电能转化为化学能 | ||
| C. | 乙装置中铜片表面有气泡生成 | D. | 甲装置中铜片表面有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
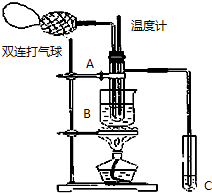 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mn2+→MnO${\;}_{4}^{-}$ | B. | NO${\;}_{3}^{-}$→NO | C. | H2→H2O | D. | Zn→Zn2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com