
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
分析 2H2S+SO2=3S+2H2O的反应中,硫化氢中硫元素失电子由-2价→0价,二氧化硫中硫元素由+4价→0价,根据氧化产物和还原产物的质量差与转移电子之间的关系式计算;分情况讨论,如果硫化氢过量计算出硫化氢和二氧化硫的物质的量,再根据二氧化硫过量计算出硫化氢和二氧化硫的物质的量.
解答 解:假设硫化氢完全反应,则硫化氢的物质的量为x,
2H2S+SO2=3S+2H2O 氧化产物和还原产物的差32g
2mol 32g
x 8g
x=0.5mol,则二氧化硫的物质的量=1mol-0.5mol=0.5mol,通入SO2和H2S的物质的量之比1:1,
假设二氧化硫完全反应,则二氧化硫的物质的量为z,
2H2S+SO2=3S+2H2O 氧化产物和还原产物的差32g
1mol 32g
y 8g
y=0.25mol,则硫化氢的物质的量为1mol-0.25mol=0.75mol,通入SO2和H2S的物质的量之比为1:3,
故选:AC.
点评 本题考查氧化还原反应的有关计算,为高频考点,侧重于学生分析、计算能力的考查,注意这两种物质不是恰好反应,有过量计算,为易错题.


科目:高中化学 来源: 题型:选择题
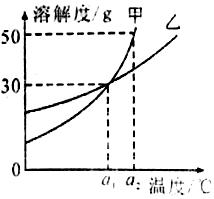
| A. | a1℃时甲和乙的饱和溶液,升温到a2℃时仍是饱和溶液 | |
| B. | 甲和乙的溶解度相等 | |
| C. | a1℃时,甲和乙各30g分别加入100g的水中,均形成饱和溶液 | |
| D. | a2℃时,在100g水中加入60g甲,形成不饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
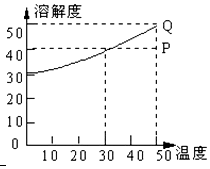 有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )
有一种盐的溶解度曲线如图,现有组成处于P点上的该溶液,下列说法错误的是(此盐不含结晶水)( )| A. | 50℃时,若该盐溶液含A克溶质,保持温度不变,加入A/4 g溶质,溶液必变成饱和溶液 | |
| B. | 50℃时,140g P点溶液最少需蒸发掉20g水才能形成饱和溶液 | |
| C. | 该溶液冷却至0℃时,析出溶质10 g | |
| D. | 在保持溶质及溶剂质量不变的情况下,使P点溶液达到饱和需降温20℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OOH的物质的量 | |
| B. | 溶液中的n(H+) | |
| C. | 用同浓度的NaOH溶液恰好完全反砬,消耗NaOH溶液的体积 | |
| D. | 溶液的导电能力 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 容器 | 温度/℃ | 物质的起始浓度/mol•L-1 | 物质的平衡浓度/mol•L-1 | ||
| c(SO2) | c(O2) | c(SO3) | c(SO3) | ||
| Ⅰ | 758 | 0.2 | 0.1 | 0 | 0.044 |
| Ⅱ | 758 | 0.1 | 0.05 | 0 | |
| Ⅲ | 858 | 0.2 | 0.1 | 0 | |
| A. | 从开始至平衡时,容器Ⅰ中SO3的反应速率为0.044 mol•L-1•s-1 | |
| B. | 平衡时,容器Ⅱ中SO3的浓度小于0.022 mol•L-1 | |
| C. | 平衡时,容器Ⅲ中SO3的浓度大于0.044 mol•L-1 | |
| D. | 若起始时,向容器Ⅰ中充入0.02 mol SO2,0.01 mol O2和0.02 mol SO3,则反应向逆反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水,它的溶度积减小、溶解度增大 | |
| B. | 升高温度,它的溶解度和溶度积都增大 | |
| C. | 饱和溶液中c(Am+)=c(Bn-) | |
| D. | 加水,它的溶度积、溶解度均不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol O2含氧原子数为0.5NA | B. | 1.8 g的NH4+中含有的电子数为NA | ||
| C. | 48 g O3含有的氧原子数为NA | D. | 1 mol H2O2中含NA个H2和NA个O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
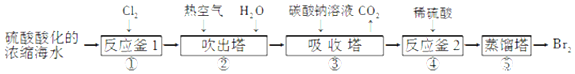
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com