
利用图示装置进行有关实验,其中能达到实验目的或得出正确结论的是
| 选项 | ① | ② | ③ | ④ | 实验目的或结论 | 装置 |
| A | 浓盐酸 | MnO2 | 干燥红色布条 | NaOH溶液 | 干燥布条不褪色 |
|
| B | 稀硝酸 | 铜粉 | 空气 | NaOH溶液 | 制备收集NO | |
| C | 浓硫酸 | 木炭 | 品红溶液 | NaOH溶液 | 浓硫酸具有氧化性 | |
| D | 浓氨水 | NaOH固体 | 空气 | 水 | 制备收集氨气 |
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
芳香族化合物A,分子式为C9H9OCl,且能发生银镜反应;D为含有八元环的芳香族化合物。A与其它物质之间的转化如下图所示:

(1)A的结构简式为 。
(2)A→E的反应条件为 ;C→D的反应类型为 。
(3)写出B→C第①步的反应方程式 。
(4)B的一种同系物F(分子式为C8H8O2)有多种同分异构体,则含有 的芳香族化合物的同分异构体有 种,写出其中核磁共振氢谱有4个峰的一种结构简式 。
的芳香族化合物的同分异构体有 种,写出其中核磁共振氢谱有4个峰的一种结构简式 。
(5)已知: 由甲苯及其它必要物质经如下步骤也可合成B:
由甲苯及其它必要物质经如下步骤也可合成B:

反应I的试剂及条件为 :反应IV所用物质的名称为 ;
反应III的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3是一种重要的化工原料,可以制备一系列物质(如图)。下列说法正确的是 ( )
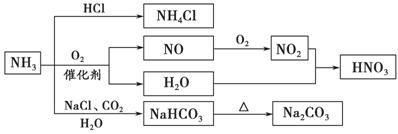
A.NH4Cl和NaHCO3都是常用的化肥
B.NH4Cl、HNO3和Na2CO3受热时都易分解
C.图中所涉及的盐类物质均可发生水解
D.NH3和NO2在一定条件下可以发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
NaCl是海水中提取出来的一种重要物质,除食用外,它还是一种工业原料,下列以NaCl为原料制得的产品(或物质)是( )
①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸
A.①②③④⑤ B.①②③④
C.①②③⑤ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
从海水中提取镁的工艺流程可表示如下:
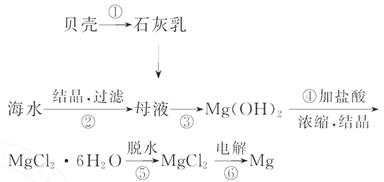
下列说法不正确的是( )
A.用此法提取镁的优点之一是原料来源丰富
B.步骤⑥电解MgCl2时阴极产生氯气
C.步骤⑤可将晶体置于HCl气体氛围中脱水
D.上述工艺流程中涉及化合、分解和复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
铁、铜等金属及其化合物在日常生产生活中用途非常广泛。
Ⅰ.孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
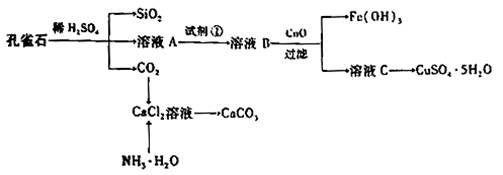
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+:从下列所给试剂中选择:实验步骤中试剂①为 (填代号),检验溶液A中Fe3+的最佳试剂为 (填代号)。
a.KMnO4 b. (NH4) 2S c. H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过 等操作。
(3)制备CaCO3时,应向CaCl2溶液中选通入(或先加入) (填化学式)。若实验过程中有氨气逸出、应选用下列 装置回收(填代号)。
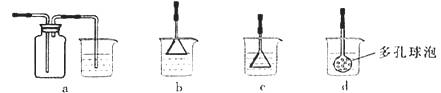
Ⅱ.(1)某同学欲从含FeCl3、FeCl2、CuCl2的废液中回收金属铜,取上述1L废液加入铁粉,充分反应。所加铁粉的物质的量与废液中铜离子的物质的量的关系曲线如图:
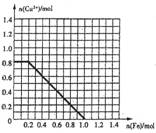 已知原废液中c(Cl-)=6.0mol.L-1,则原废液中c(Fe3+)= ,c(Fe2+)= 。(忽略水解及溶液体积变化)
已知原废液中c(Cl-)=6.0mol.L-1,则原废液中c(Fe3+)= ,c(Fe2+)= 。(忽略水解及溶液体积变化)
(2)现有Fe2O3、ZnO、CuO的混合固体粉末ag,在加热条件下用足量的CO还原,得到金属混合物2.41g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀。请回答下列问题:
①a= 。
②若agFe2O3、ZnO、CuO的混合物总物质的量为bmol,则Fe2O3的物质的量为 。(用含b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,常用于水的消毒以及纺织高漂白。过氧化氢法生产亚氯酸钠的流程图如下

已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O且NaClO2在碱性条件下稳定性较高。试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为
(2)在NaClO2稳定装置中,H2O2作 (选填序号)。
A.氧化剂 B.还原剂
C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
(3)在实验室模拟“固体分离装置”中的技术,必须进行的实验操作是 (按实验后顺序填写操作代号)。
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却
(4)经查阅资料知道:当pH≤2.0时,ClO-2能被I完全还原成Cl—;
溶液中Na2S2O3能与I2反应生成NaI和Na2S4O6。
欲测定成品中NaClO2的含量,现进行如下操作:

①步骤Ⅱ中发生反应的离子方程式是 ,
步骤Ⅲ中达到滴定终点时的现象是 。
②若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数 (用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
.下列说法正确的是( )
A.用25ml量筒量取12.3ml盐酸;用托盘天平称取8.75g食盐
B.用pH试纸测得某氯水的pH为2;用标准NaOH溶液滴定未知浓度的盐酸,用去NaOH溶液23.10ml
C.将质量分数为5%和25%的氨水等体积混合后,所得溶液中溶质的质量分数大于15%
D.浓硝酸必须保存在棕色玻璃瓶中;钠必须保存在煤油中
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列三个热化学方程式
①H2(g)+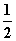 O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
③C(s)+H2O(g)===CO(g)+H2(g) ΔH=131 kJ·mol-1
写出碳燃烧生成CO和CO燃烧的热化学方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com