
设阿伏加德罗常数为NA,下列说法正确的是( )
A.5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA
B.1 mol NH3含有的电子数10NA
C.常温常压下,22.4L的氧气含氧原子数为2NA
D.常温下,1L0.1mol/L AlCl3溶液中含Al3+ 数为0.1NA
 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源:物理教研室 题型:022
黄铁矿![]() Fe2(SO4)3
Fe2(SO4)3
CO2+H2O![]() C6H12O6
C6H12O6
(1)①从生物代谢过程看,b过程属________作用。
②氧化亚铁硫杆菌的代谢类型是________。
A.自养需氧型 B.异氧需氧型
C.自养厌氧型 D.异氧厌氧型
(2)写出a过程的化学方程式_________________。
(3)人们可以利用Fe2(SO4)3作氧化剂溶解铜矿石(Cu2S),然后,加入铁屑进一步得到铜,请写出其离子方程式___________________________。
(4)下列不属于细菌冶金特点的是_____________________。
A.对贫矿、尾矿的开采更有价值
B.中间产物FeSO4和S可再次被细菌氧化为Fe2(SO4)3和H2SO4,因此可循环使用
C.所有的细菌来源广泛,很容易找到并大规模培养
D.能大大降低能源消耗,减少污染
(5)工业上可利用粗铜(含Zn、Ag、Au)等经电解制备精铜,电解过程中,精铜接电源的________极,粗铜上的电极反应________。
(6)某工厂按上述(5)原理,平均每秒生产Amol Cu(设阿伏加德罗常数为N,电子电量为e库仑),求电解槽中的平均电流________。
查看答案和解析>>
科目:高中化学 来源: 题型:022
“细菌冶金”是利用某些细菌的特殊代谢功能开采矿石,例如,在氧化亚铁硫杆菌的存在下,黄铁矿被空气氧化为Fe2(SO4)3,并使溶液酸性增强,其过程如下:
黄铁矿![]() Fe2(SO4)3
Fe2(SO4)3
CO2+H2O![]() C6H12O6
C6H12O6
(1)①从生物代谢过程看,b过程属________作用。
②氧化亚铁硫杆菌的代谢类型是________。
A.自养需氧型 B.异氧需氧型
C.自养厌氧型 D.异氧厌氧型
(2)写出a过程的化学方程式_________________。
(3)人们可以利用Fe2(SO4)3作氧化剂溶解铜矿石(Cu2S),然后,加入铁屑进一步得到铜,请写出其离子方程式___________________________。
(4)下列不属于细菌冶金特点的是_____________________。
A.对贫矿、尾矿的开采更有价值
B.中间产物FeSO4和S可再次被细菌氧化为Fe2(SO4)3和H2SO4,因此可循环使用
C.所有的细菌来源广泛,很容易找到并大规模培养
D.能大大降低能源消耗,减少污染
(5)工业上可利用粗铜(含Zn、Ag、Au)等经电解制备精铜,电解过程中,精铜接电源的________极,粗铜上的电极反应________。
(6)某工厂按上述(5)原理,平均每秒生产Amol Cu(设阿伏加德罗常数为N,电子电量为e库仑),求电解槽中的平均电流________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)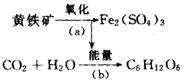 “细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如氧化亚铁硫杆菌在溶液中能将黄铁矿氧化为Fe2(SO4)3,并使溶液酸性增强,其过程如下:
“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如氧化亚铁硫杆菌在溶液中能将黄铁矿氧化为Fe2(SO4)3,并使溶液酸性增强,其过程如下:
1.(1)从生物代谢看,(b)过程属 作用;
(2)氧化亚铁硫杆菌的代谢类型应是 。
2.写出(a)过程的化学反应方程式。
3.人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,请你写出其离子反应方程式。
4.工业上可利用粗铜(含Zn、Ag、Au等)经电解制得精铜(电解铜)。写出电解过程中的电极材料和电极反应。某工厂按此原理,平均每秒生产A mol精铜,求电解机槽中平均电流强度。(设阿伏加德罗常数为 N,每个电子带电量为e C)
5.请评价细菌冶金的优点。
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数为N。。则下列说法正确的是 ( )
A.7.1g Cl2与足量NaOH溶液充分反应后,转移的电子数为O.1 NA
B.1.0L浓度为1.0 mol·L-1的一元酸溶液中含有的氢离子数为1.0 N2
C.常温下,1L 0.1 mo1.L-1的NH4NO2溶液中氮原子数小于0.2 NA
D.标准状况下,22.4L乙醛中含有的氧原子数为1.0 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com