
【题目】按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热化学方程式____。
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热化学方程式_____。
(3)已知下列热化学方程式:①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol;
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ/mol;
③2H2(g)+O2(g)=2H2O(l ) ΔH3=-571.6kJ/mol,
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式_________。
【答案】![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol C4H10(g)+
Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol C4H10(g)+![]() O2(g)= 4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol 2C(s)+2H2(g)+O2(g)=CH3COOH(l)ΔH=-488.3 kJ/mol
O2(g)= 4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol 2C(s)+2H2(g)+O2(g)=CH3COOH(l)ΔH=-488.3 kJ/mol
【解析】
(1)根据中和热的概念:稀的强酸和强碱反应生成1mol水所放出的热量求出中和热并书写出中和热的热化学方程式。
(2)根据生成碳酸钙的质量计算丁烷的物质的量,结合燃烧热的概念书写表示丁烷燃烧热化学方程式;
(3)利用盖斯定律计算反应热,并书写热化学方程式。
(1)1mol H2SO4溶液与足量NaOH溶液完全反应,放出114.6kJ的热量,即生成2mol水放出114.6kJ的热量,反应的反应热为-114.6kJ/mol,中和热为-57.3kJ/mol,则中和热的热化学方程式:![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol;
Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol;
(2)n(CaCO3)=![]() =0.25mol,则根据C元素守恒,可知n(CO2)=0.25mol,即丁烷燃烧生成的二氧化碳为0.25mol,由丁烷燃烧的化学方程式2C4H10+13O2=8CO2+10H2O可知反应的丁烷的物质的量是n(C4H10)=
=0.25mol,则根据C元素守恒,可知n(CO2)=0.25mol,即丁烷燃烧生成的二氧化碳为0.25mol,由丁烷燃烧的化学方程式2C4H10+13O2=8CO2+10H2O可知反应的丁烷的物质的量是n(C4H10)=![]() =
=![]() mol,因为燃烧
mol,因为燃烧![]() mol的丁烷放出的热量为Q,所以燃烧1mol丁烷产生CO2气体和产生液态水放出热量是16QkJ,故丁烷的燃烧热为16QkJ,所以表示丁烷燃烧热化学方程式为C4H10(g)+
mol的丁烷放出的热量为Q,所以燃烧1mol丁烷产生CO2气体和产生液态水放出热量是16QkJ,故丁烷的燃烧热为16QkJ,所以表示丁烷燃烧热化学方程式为C4H10(g)+![]() O2(g)= 4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol;
O2(g)= 4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol;
(3)已知:CH3COOH(l)+2O2(g)= 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol;
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ/mol;
③2H2(g)+O2(g)=2H2O(l ) ΔH3=-571.6kJ/mol,
利用盖斯定律将②×2+③×2-①可得:
2C(s)+2H2(g)+O2(g)=CH3COOH(l);△H=2×(-393.5kJ/mol)+2×(-285.8kJ/mol)-(-870.3kJ/mol)=-488.3kJ/mol,
所以热化学方程式为2C(s)+2H2(g)+O2(g)=CH3COOH(l)ΔH=-488.3 kJ/mol。


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】如图是我国学者研发的高效过氧化氢——尿素电池的原理装置,该装置工作时,下列说法错误的是
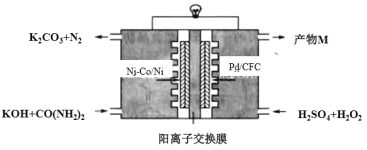
A.Ni-Co/Ni极上的电势比Pd/CFC极上的高
B.向正极迁移的主要是K+,产物M主要为K2SO4
C.负极反应为:CO(NH2)2+8OH–-6e–=CO32-+N2↑+6H2O
D.Pd/CFC极上发生反应:H2O2+2e–=2OH–
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂海水电池的反应原理为:2Li+2H2O=2LiOH+H2↑,其示意图如图所示。有关该电池工作时说法错误的是

A.金属锂作正极
B.镍电极上发生还原反应
C.海水作为电解质溶液
D.可将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)所含铁元素只有还原性的物质是_________。
A.Fe B.FeCl2 C.FeCl3 D.Fe2O3
(2)当人体缺铁时,往往要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:____________________________________________________________________。
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有________________(填化学性质)。
(3)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:
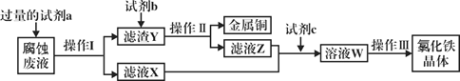
回答下列问题:
①试剂a是___________,操作I用到的玻璃仪器有烧杯、玻璃棒和___________。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________。
③上述流程中操作III包括________________、________________、过滤、洗涤。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反-2-己烯醛(D)是一种重要的合成香料,下列合成路线是制备D的方法之一。根据该合成路线回答下列问题:
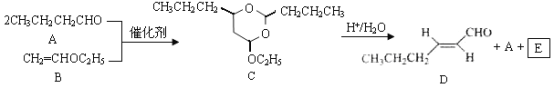
已知: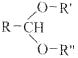
![]() RCHO+R'OH+R"OH
RCHO+R'OH+R"OH
(1)A的名称是__________;B分子中共面原子数目最多为__________;C分子中与环相连的三个基团中,不同化学环境的氢原子共有__________种。
(2)D中含氧官能团的名称是__________,写出检验该官能团的化学反应方程式:__________。
(3)E为有机物,能发生的反应有__________。
a.聚合反应b.加成反应c.消去反应d.取代反应
(4)B的同分异构体F与B有完全相同的官能团,写出F所有可能的结构:________。
(5)以D为主要原料制备己醛(目标化合物),在方框中将合成路线的后半部分补充完整。
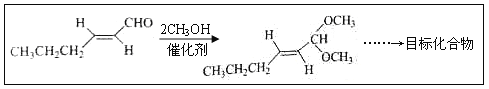
(6)问题(5)的合成路线中第一步反应的目的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠通常保存在_________中,加热时,钠可以在空气中_________,发出________火焰,生成____________色固体。化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,体积均为100mL、浓度均为的两种一元碱MOH和ROH的溶液中,分别通入HCl气体,![]() 随通入HCl的物质的量的变化如图所示。下列有关说法中不正确的是(不考虑溶液体积的变化)( )
随通入HCl的物质的量的变化如图所示。下列有关说法中不正确的是(不考虑溶液体积的变化)( )
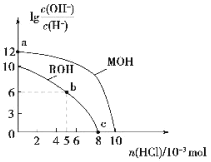
A.MOH是强碱,ROH是弱碱
B.a点由水电离产生的c(H+)和c(OH-)的乘积为1×10-26
C.b点溶液中:c(Cl-)>c(R+)>c(H+)>c(OH-)
D.c点溶液的pH=7,且所含溶质为ROH和RCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pBa=-lgc(Ba2+),Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=3.0×10-9。常温下,用 0.1 mol·L-1Na2SO4溶液滴定 20 mL 0.1 mol·L-1BaCl2溶液的曲线如图所示,V0达到滴定终点,下列说法错误的是
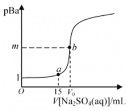
A.图像中,m=5,V0=20
B.若将c(BaCl2)从 0.1 mol· L-1变为 0.2 mol· L-1,m 值将减小
C.a 点溶液中离子浓度大小关系为:c(Cl-)>c(Na+)>c(Ba2+)>c(OH-)
D.向b点溶液中滴加Na2CO3溶液至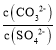 ≥30 时将生成BaCO3
≥30 时将生成BaCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com