
| A、A是固体,C是气体,正反应吸热 |
| B、A是气体,C是固体或液体,正反应放热 |
| C、A是气体,C是气体,正反应放热 |
| D、A是气体,C是气体,正反应吸热 |


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
| A、硫离子的核外电子排布式:1s22s22p63s23p6 |
| B、N2的结构式::N≡N: |
C、NaCl的电子式: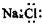 |
D、CO2的分子模型示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①③④ |
| C、②④⑤ | D、①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2+的核外电子排布式为1s22s22p63s23p64s2 |
B、铁原子的价电子轨道排布图: |
| C、某原子的核外电子排布式为1s22s22p63s23p63d54s1,则其成单电子数为2 |
| D、各能级的原子轨道数按s,p,d,f的顺序依次为1、3、5、7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 0℃ | 10℃ | 20℃ | 30℃ |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.1 |
| NH4HCO3 | 11.9 | 15.9 | 21.0 | 27.0 |
| NaHCO3 | 6.9 | 8.15 | 9.6 | 11.1 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 |
| A、NH4Cl |
| B、NH4HCO3 |
| C、NaHCO3 |
| D、NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、K+、Fe2+、NO3- |
| B、NH4+、Na+、NO3-、S2- |
| C、K+、NH4、NO3-、Cl- |
| D、Mg2+、Fe3+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向正反应方向移动 |
| B、A的转化率增大了 |
| C、a<b |
| D、B的质量分数减少了 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、燃烧后能生成CO2和H2O的有机物,一定含有碳、氢、氧三种元素 |
| B、所有烷烃中均有碳碳单键 |
| C、属于同分异构体的物质,其分子式相同,分子量相同;但分子量相同的不同物质不一定是同分异构体 |
| D、分子组成相差一个或几个CH2原子团的物质是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、α鸢尾酮可与某种酚互为同分异构体 |
| B、1 mol α鸢尾酮最多可与3 mol H2加成 |
| C、α鸢尾酮能发生银镜反应 |
D、α鸢尾酮经加氢→消去→加氢可转变为 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com