
分析 纤维分天然纤维和化学纤维,天然纤维是自然界原有的或经人工培植的植物上、人工饲养的动物上直接取得的纺织纤维,是纺织工业的重要材料来源.化学纤维又可分为合成纤维和人造纤维,合成纤维是由人工合成方法制得的,生产不受自然条件的限制,人造纤维是用木材、草类的纤维经化学加工制成的粘胶纤维,据此分析解答.
解答 解:化学纤维又可分为合成纤维和人造纤维,合成纤维是由人工合成方法制得的,生产不受自然条件的限制,人造纤维是用木材、草类的纤维经化学加工制成的粘胶纤维,所以通过化学方法将木材等含有天然纤维素的物质加工而成的纤维,称为人造纤维,利用石油、天然气等做原料制成单体,然后再经过化学合成和机械加工等制成的纤维,称为合成纤维,
故答案为:人造纤维;合成纤维.
点评 本题主要考查学生对合成材料的认识.侧重考查学生对人造纤维和合成纤维的特点的认识和区别能力,掌握人造纤维和合成纤维的特征是正确解答此类题的关键,题目难度不大.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L乙烯含有的共用电子对数为5NA | |
| B. | lmolNaHSO4中的阳离子数为2NA | |
| C. | 通常状况下,lmolNO和0.5molO2在密闭容器中混合,生成NO2分子数为NA | |
| D. | 制取漂白粉时,标准状况下22.4LC12参加反应,转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上可用铝热反应大规模炼铁 | B. | SO2常用于纸张等植物纤维的漂白 | ||
| C. | Si是重要的半导体材料 | D. | 电解熔融MgCl2,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
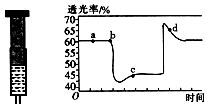
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH (g)和 1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对盛在烧杯(敞口)内的氨水加热,氨水中NH4+浓度减小 | |
| B. | 对2HI(g)?H2(g)+I2(g),保持容器体积不变,通入氢气可使平衡体系颜色变浅 | |
| C. | 500℃左右比室温更有利于合成氨的反应 | |
| D. | 高压有利于合成氨的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>②>③>① | B. | ①>④>②>③ | C. | ①>②>③>④ | D. | ④>①>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
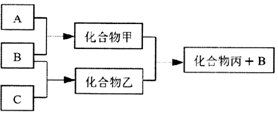 如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )| A. | Z元素位于第二周期第VIA族 | |
| B. | 可用排水法收集化合物乙 | |
| C. | 元素X、Y、Z的原子半径大小关系为X<Z<Y | |
| D. | 化合物甲溶于化合物丙中,存在的微粒有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
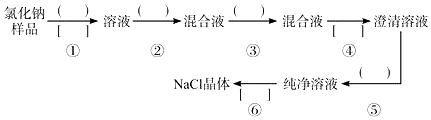
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com