
【题目】分别将足量下列气体通入稀Na2S溶液中,可以使溶液变浑浊的是( )
A. CO B. SO2 C. HCl D. CO2
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】有机物G是合成新农药的重要中间体。以化合物A为原料合成化合物G的工艺流程如下:

(1)化合物G中含氧官能团的名称为 。
(2)反应E→F的类型为 。
(3)化合物B的分子式为C7H6Cl2,B的结构简式为 。
(4)写出同时满足下列条件的D的一种同分异构体的结构简式: 。
①能发生银镜反应;
②能水解,且水解产物之一能与FeCl3溶液发生显色反应;
③分子中只有3种不同化学环境的氢。
(5)请以化合物F和CH2(COOC2H5)2为原料制备 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干) 。
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100 mol·L1的NaOH溶液分别滴定10.00 mL浓度均为0.100 mol·L1 的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
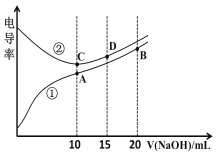
A.曲线①代表滴定HCl溶液的曲线
B.A点溶液中:c(CH3COO)+c(OH)c(H+)=0.1 molL1
C.在相同温度下,A、B、C三点溶液中水的电离程度:C<B<A
D.D点溶液中:2c(Na+)=3c(Cl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义。
(1)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
已知:用CO(g)还原NO2(g)的能量转化关系如图所示。
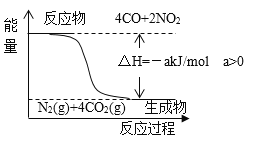
若用标准状况下22.4LCO,还原NO2至N2(CO完全反应)的整个过程中,转移电子的物质的量为_______mol,放出的热量为_______kJ(用含有a的代数式表示)。
(2)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若1molCH4还原NO2至N2和液态水,整个过程中放出的热量为867kJ,则△H2=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列制备金属单质的方法或原理正确的是 ( )。
A. 在高温条件下,用H2还原MgO制备单质Mg
B. 在通电条件下,电解熔融Al2O3制备单质Al
C. 在通电条件下,电解饱和食盐水制备单质Na
D. 加强热,使CuO在高温条件下分解制备单质Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物的描述正确的是
A. 有机物是生命特有的物质
B. 有机物只能由动植物体内产生,不能用人工方法合成
C. 凡是含碳元素的化合物都属于有机物
D. 在所有的有机物中都含有碳;多数含有氢,其次还含有氧、氮、卤素、硫等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液.
②按下图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
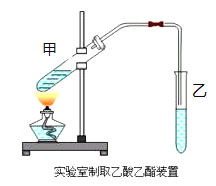
(1)写出制取乙酸乙酯的化学方程式:___________________________________。
(2)在反应未开始前,乙试管中所盛溶液为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
(1)CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2]。
已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式:______________。
(2)CO2与H2也可用于合成甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中压强为P时,该反应在不同温度、不同投料比时,达平衡时CO2的转化率如图一所示。
CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中压强为P时,该反应在不同温度、不同投料比时,达平衡时CO2的转化率如图一所示。
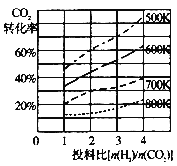
图一 图二 图三
①该反应的S 0,H 0(填“>”或“<”)。
②700K时,用平衡分压代替平衡浓度表示的化学平衡常数KP= 。
③若温度不变,减小反应物投料比[n(H2)/n(CO2)],K值 (填“增大”、“减小”或“不变”)。
④700K投料比[n(H2)/n(CO2)] = 2时,达平衡时H2的转化率为 。
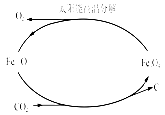
(3)利用太阳能和缺铁氧化物[如Fe0.9O]可将富集到的廉价CO2热解为碳和氧气,实现CO2再资源化,转化过程如图二所示,若用1mol缺铁氧化物[Fe0.9O]与足量CO2完全反应可生成 molC(碳)。
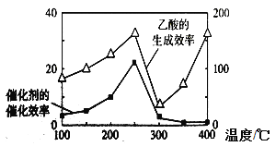
(4)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图三。如何解释图中250-400℃时温度升高与乙酸的生成速率变化的关系? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com