
| A、Cu(OH)2+HCl;NaOH+HNO3 |
| B、NaHCO3+H2SO4;Na2CO3+HCl |
| C、NaHSO4+NaOH;H2SO4+NaOH |
| D、BaCl2+H2SO4;Ba(OH)2+H2SO4 |


科目:高中化学 来源: 题型:
| A、滤液中一定有Fe(NO3)3 |
| B、滤渣只含Ag和Cu,一定无Zn |
| C、滤渣中一定有Ag、Cu和Fe,一定无Zn |
| D、滤渣中可能有Ag、Cu、Fe和Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、这一定是自发反应 |
| B、该反应需要加热 |
| C、生成物的总能量低于反应物的总能量 |
| D、反应物比生成物更稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10gH2和10gO2 |
| B、22.4LN2和32gO2 |
| C、9g H2O和0.5molCl2 |
| D、3.01×1023个氢分子和0.1molN2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4LH2含有的分子数为1 NA |
| B、常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C、通常状况下,1 NA个 CO2分子占有的体积为22.4L |
| D、1L0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
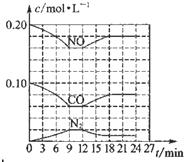 将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H<0在不同条件下,反应过程中部分物质的浓度变化如图所示.下列说法正确的是( )
将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H<0在不同条件下,反应过程中部分物质的浓度变化如图所示.下列说法正确的是( )| A、容器内的压强不发生变化说明该反应达到平衡 |
| B、当向容器中再充入0.20 mol NO时,平衡向正反应方向移动,K增大 |
| C、第12 min时改变的反应条件为减小压强 |
| D、向该容器内充入He气,容器内气体压强增大,所以反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用醋酸除水垢:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- | ||
B、氯乙酸与氢氧化钠溶液共热:ClCH2COOH+OH-
| ||
C、乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:CH3CHO+2Cu(OH)2+OH-
| ||
D、服用阿司匹林过量出现水杨酸(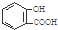 )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: +2 HCO3-→ +2 HCO3-→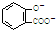 +2 CO2↑+2 H2O +2 CO2↑+2 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| HCl |
| 实 验 序 号 | 初始浓度c/mol?L-1 | 溴颜色消失 所需时间t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.80 | 0.20 | 0.0010 | 290 |
| ② | 1.60 | 0.20 | 0.0010 | 145 |
| ③ | 0.80 | 0.40 | 0.0010 | 145 |
| ④ | 0.80 | 0.20 | 0.0020 | 580 |
| A、增大c(Br2),v(Br2)增大 |
| B、实验②和③的v(Br2)相 |
| C、增c(HCl),v(Br2)增大 |
| D、增大c(CH3COCH3),v(Br2)增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com