
| A. | 相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol•L-1盐酸、③0.1 mol•L-1氯化镁溶液、④0.1 mol•L-1硝酸银溶液中,Ag+浓度:①>④=②>③ | |
| B. | 将NH4HCO3、AlCl3、FeCl2、KAl(SO4)2的溶液分别加热蒸干、灼烧,均不能得到原物质 | |
| C. | 可直接根据Ksp的数值大小比较难溶物在水中的溶解度大小 | |
| D. | 25℃时,Ksp(AgCl)>Ksp(AgI),向AgCl的悬浊液中加入KI固体,有黄色沉淀生成 |
分析 A.由AgCl(s)?Ag+(aq)+Cl-(aq)可知,加硝酸银时Ag+浓度增大,加含氯离子的物质平衡逆向移动导致Ag+浓度减小;
B.KAl(SO4)2的溶液加热蒸干、灼烧,能得到原物质;
C.同类型的难溶电解质,由Ksp的数值大小比较难溶物在水中的溶解度大小;
D.向AgCl的悬浊液中加入KI固体,有黄色沉淀生成,发生沉淀的转化.
解答 解:A.由AgCl(s)?Ag+(aq)+Cl-(aq)可知,加硝酸银时Ag+浓度增大,加含氯离子的物质平衡逆向移动导致Ag+浓度减小,②③相比,③中氯离子浓度大,则③中银离子浓度最小,即Ag+浓度:④>①>②>③,故A错误;
B.KAl(SO4)2的溶液加热蒸干、灼烧,能得到原物质,AlCl3水解生成的盐酸易挥发,FeCl2易被氧化、且水解生成的盐酸易挥发,NH4HCO3加热易分解,不能得到原物质,故B错误;
C.同类型的难溶电解质,由Ksp的数值大小比较难溶物在水中的溶解度大小,如AgCl、AgI可由Ksp比较溶解度,不同类型的难溶电解质不能直接比较,故C错误;
D.向AgCl的悬浊液中加入KI固体,有黄色沉淀生成,发生沉淀的转化,则Ksp(AgCl)>Ksp(AgI),故D正确;
故选D.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握平衡移动、Ksp的应用、沉淀转化为解答该题的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×l0-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | NaHCO3溶液中,c(Na+)>c(HCO3-)>c(H2CO3)>c(OH-) | |
| B. | 将amol•L-1HCN溶液与amol•L-1NaOH溶液等体积混合后,测得所得溶液显碱性,则c(CN-)>c(Na+) | |
| C. | 等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) | |
| D. | 1.0 mol•L-1Na2CO3溶液:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当2a=b时,溶液中生成的沉淀质量最大 | |
| B. | 当a=2b时,发生的离子反应为2NH4++SO42-+Ba2++2OH-═BaSO4↓+2NH3•H2O | |
| C. | 当2b≤3a时,发生的离子反应为3SO42-+2Al3++3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| D. | 当2a<b≤2.5a时,溶液中的n(AlO2-)为0.02(b-2a) mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用过量石灰乳吸收工业尾气中的SO2:Ca2++2OH-+SO2═CaSO3↓+H2O | |
| B. | 用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用铜做电极电解NaCl溶液:2C1-+2 H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| D. | 将 Fe2O3 加入到 HI 溶液中:Fe2O3+6H+═2Fe3++3 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物共有5种 | |
| B. | 菲的结构简式如图 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 | |
| C. | 与 互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 | |
| D. | 某饱和链烃,分子中含有5个碳原子的,其一氯取代物共有8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
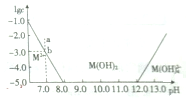
| A. | M(OH)2属于两性氢氧化物 | |
| B. | 沉淀分离M2+需控制pH在8~12之间 | |
| C. | 升高温度,可以实现从b点移动到a点 | |
| D. | 室温时,M(OH)2(s)的溶度积常数为1×10-17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | HCOOH | HCN | H2S |
| 电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| A. | NaHS溶液中加入适量KOH后:c(Na+)═c(H2S)+c(HS-)+2C(S2-) | |
| B. | HCOO-、CN-、HS-在溶液中不可以大量共存 | |
| C. | 等体积、等浓度的HCOONa和NaCN两溶液中所含离子数目前者大于后者 | |
| D. | 恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com