
下列电离方程式的书写正确的是( )
A.NH4++H2O NH3·H2O+H+
NH3·H2O+H+
B.S2-+2H2O H2S+2OH-
H2S+2OH-
C.CH3COOH+H2O CH3COO-+H3O+
CH3COO-+H3O+
D.CH3COOH+OH- CH3COO-+H2O
CH3COO-+H2O
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源:2015届吉林省高二3月月考化学试卷(解析版) 题型:选择题
在酯化反应和酯的水解反应中硫酸的作用分别是
A.催化剂、脱水剂;催化剂 B.催化剂、吸水剂;催化剂
C.都作催化剂 D.吸水剂;催化剂
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题9有机化合物的获取与应用练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.纤维素和淀粉遇碘水均显蓝色
B.蛋白质、乙酸和葡萄糖均属电解质
C.溴乙烷与NaOH乙醇溶液共热生成乙烯
D.乙酸乙酯和食用植物油均可水解生成乙醇
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题8溶液中的离子反应练习卷(解析版) 题型:选择题
物质的量浓度相等的4种溶液:①H2S、②NaHS、③Na2S、④H2S和NaHS的混合液。下列说法正确的是( )
A.溶液pH由大到小的顺序:③>②>①>④
B.c(H2S)由大到小的顺序:①>④>②>③
C.在Na2S溶液中:2c(Na+)=c(H2S)+c(HS-)+c(S2-)
D.在NaHS溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-)
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题8溶液中的离子反应练习卷(解析版) 题型:选择题
25°C时,在1.0 L浓度均为0.01 mol·L-1的某一元酸HA与其钠盐组成的混合溶液中,测得c(Na+)>c(A-),则下列描述中,不正确的是( )
A.该溶液的pH<7
B.HA的酸性很弱,A-水解程度较大
C.c(A-)+c(HA)=0.02 mol·L-1
D.n(A-)+n(OH-)=0.01 mol+n(H+)
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:填空题
甲醇可以与水蒸气反应生成氢气,反应方程式如下:
CH3OH(g)+H2O(g)  CO2(g)+3H2(g) ΔH>0
CO2(g)+3H2(g) ΔH>0
(1)一定条件下,向体积为2 L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),20 s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为________。
(2)判断(1)中可逆反应达到平衡状态的依据是(填序号)________。
①v正(CH3OH)=v正(CO2)
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④CH3OH、H2O、CO2、H2的浓度都不再发生变化
(3)下图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1 mol CH3OH(g)和2 mol H2O(g),向B容器中充入1.2 mol CH3OH(g)和2.4 mol H2O(g),两容器分别发生上述反应。已知起始时容器A和B的体积均为a L。试回答:
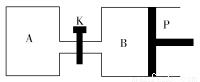
①反应达到平衡时容器B的体积为1.5aL,容器B中CH3OH转化率为________,A、B两容器中H2O(g)的体积百分含量的大小关系为:B(填“>”“<”或“=”)________A。
②若打开K,一段时间后重新达到平衡,容器B的体积为________L(连通管中气体体积忽略不计,且不考虑温度的影响)。
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:选择题
将一定量A、B装入容积为1 L的恒温密闭容器中,发生反应:2A(g)+bB(g)  cC(g),1 min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的
cC(g),1 min时达到平衡,C的浓度为x mol·L-1。若保持温度不变,将密闭容器的容积压缩为原来的 ,重新达到平衡后,C的浓度为2.5 x mol·L-1,下列说法正确的是 ( )
,重新达到平衡后,C的浓度为2.5 x mol·L-1,下列说法正确的是 ( )
A.化学计量数的关系:b<c
B.容器的容积减小后,该反应的逆反应速率减小
C.原容器中用B的浓度变化表示该反应在1 min内的速率为 mol·(L·min)-1
mol·(L·min)-1
D.若保持温度和容器的容积不变,充入氦气(不参与反应),平衡不发生移动
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题6化学反应与能量变化练习卷(解析版) 题型:选择题
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1 mol时,下列说法不正确的是( )
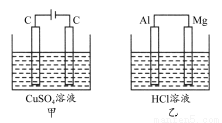
A.溶液的质量变化:甲减小乙增大
B.溶液pH变化:甲减小乙增大
C.相同条件下产生气体的体积:V甲=V乙
D.电极反应式:甲中阴极为Cu2++2e-=Cu,乙中负极为Mg-2e-=Mg2+
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题3从矿物到基础材料练习卷(解析版) 题型:填空题
甲、乙、丙、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)
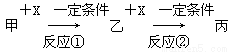
试回答下列问题:
(1)若X是强氧化性单质,则甲可能是__________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向丙的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀。则乙的化学式为________________;丙溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)__________________________。
(3)若甲、乙、丙为含有金属元素的无机化合物,X为强电解质,甲溶液与丙溶液反应生成乙;反应①的离子方程式为____________________,或____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com