
| A. | 体积为1L、浓度为1mol/L的H2SO4和H3PO4溶液中所含氧原子数目均为4NA | |
| B. | 1molFe在71g Cl2中完全燃烧转移的电子数为3NA | |
| C. | 25℃时,pH=13的NaOH溶液中含有OH-的数目为NA | |
| D. | 25℃、101KPa下,22.4L氯气通入NaOH溶液中充分反应,转移的电子数小于NA |
分析 A.溶剂水分子中也含有氧原子;
B.71g氯气的物质的量为2mol,2mol氯气完全反应最多达到2mol电子;
C.缺少溶液体积,无法计算溶液中含有氢氧根离子的数目;
D.25℃、101KPa下气体摩尔体积大于22.4L/mol,22.4L的氯气的物质的量小于1mol.
解答 解:A.由于水分子中含有O原子,则无法计算溶液中含有氧原子的我知道及数目,故A错误;
B.Fe与氯气反应生成氯化铁,71g氯气的物质的量为2mol,2mol氯气完全反应最多达到2mol电子,则二者完全燃烧转移的电子数为2NA,故B错误;
C.没有告诉pH=13的NaOH溶液的体积,无法计算溶液中含有氢氧根离子的物质的量及数目,故C错误;
D.25℃、101KPa下22.4L氯气的物质的量小于$\frac{22.4L}{22.4L/mol}$=1mol,该氯气通入NaOH溶液中充分反应转移电子小于1mol,则转移的电子数小于NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的计算与判断,题目难度中等,注意掌握物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | B元素的简单气态氢化物与E的氢化物化合,生成物的水溶液呈酸性 | |
| B. | B、C、E最高价氧化物对应的水化物溶液均能与D元素的氧化物反应 | |
| C. | 元素B、E分别与元素A构成的含有18个电子的分子中均含有非极性共价键 | |
| D. | 最高价氧化物对应水化物的碱性:C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 .
.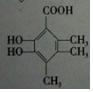 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 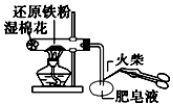 验铁粉与水蒸气反应产生的氢气 | |
| B. |  分离两种互溶但沸点相差较大的液体混合物 | |
| C. |  乙酸乙酯的制备演示实验 | |
| D. |  碳酸氢钠受热分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH)n,己知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH)n,己知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )| A. | 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 | |
| B. | 在Mg-空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 | |
| C. | M-空气电池放电过程的正极反应式:正极反应式为O2+2H2O+4e-═4OH- | |
| D. | 比较Mg、Al、Zn三种金属-空气电池,Mg-空气电池的理论比能量最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 将稀盐酸滴入加有酚酞的Na2SiO3溶液中,边加边震荡, | 红色变浅并接近消失 | 有硅酸胶体生成 |
| B | 氯化钠晶体导电实验 | 不导电 | 晶体不存在离子 |
| C | AgI悬浊液中滴入Na2S溶液 | 固体变黑 | Ksp(Ag2S)>Ksp(AgI) |
| D | 测量H2CO3的电离常数 | Ka1>ka2 | H2CO3一级电离常数产生的H+对二级电离起抑制作用 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水.下列说法中不正确的是( )
甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.乙图是一种家用环保型消毒液发生器,用惰性电极电解饱和食盐水.下列说法中不正确的是( )| A. | N电极上每消耗22.4L气体(标准状况)时,则有4molH+通过质子交换膜从负极区移向正极区 | |
| B. | 若装置乙所需的电能来自装置甲,则b极应与X 极连接 | |
| C. | 若有机废水中主要含有葡萄糖,则装置甲中M极发生的电极应为C6H12O6+6H2O-24e-=6CO2↑+24H+ | |
| D. | 由装置乙制得的家用消毒液的主要成分是NaClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | B. | 2CH3CH2OH+O2$\stackrel{Cu,△}{→}$2CH3CHO+2H2O | ||
| C. |  | D. |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com