
| A. | CuSO4溶液中加入过量氨水得到深蓝色溶液:Cu2++2OH-═Cu(OH)2↓ | |
| B. | 碳酸钠溶液中滴入酚酞试液,溶液变红:CO32-+2H2O?H2CO3+2OH- | |
| C. | FeCl2溶液中加入K3[Fe(CN)6]溶液,生成蓝色沉淀:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓ | |
| D. | 90℃时,测得纯水pH=6.7,pH<7的原因是:H2O(l)?H+(aq)+OH-(aq)△H<0 |
分析 A.加入过量氨水,反应生成[Cu(NH3)4]2+;
B.水解分步进行,以第一步为主;
C.生成蓝色沉淀为Fe3[Fe(CN)6]2;
D.升高温度促进水的电离.
解答 解:A.CuSO4溶液中加入过量氨水得到深蓝色溶液的离子反应为Cu2++4NH3.H2O═4H2O+[Cu(NH3)4]2+,故A错误;
B.碳酸钠溶液中滴入酚酞试液,溶液变红的离子反应为CO32-+H2O?HCO3-+OH-,故B错误;
C.FeCl2溶液中加入K3[Fe(CN)6]溶液,生成蓝色沉淀的离子反应为3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓,故C正确;
D.90℃时,测得纯水pH=6.7,pH<7的原因是:H2O(l)?H+(aq)+OH-(aq)△H>0,故D错误;
故选C.
点评 本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、水解反应的考查,注意选项C为解答的难点,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

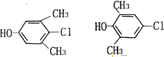 (写两种)
(写两种) 的化学方程式
的化学方程式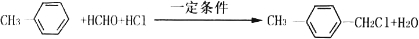 ,
,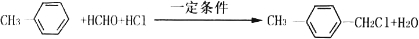 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X在周期表中的位置为第2周期VIA族 | |
| B. | 1 mol甲与足量的乙完全反应转移的电子数为6.02×1023 | |
| C. | 元素X、Y、Z的原子半径由大到小的顺序为r(Z)>r(Y)>r(x) | |
| D. | 1.0 L 0.1 mol•L-1戊溶液中阴离子的总物质的量小于0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| B. | 物质的量浓度相等的①(NH4)2SO4溶液、②NH4HCO3溶液、③NH4Cl 溶液、④(NH4)2Fe(SO4)2溶液中,c(${NH}_{4}^{+}$)的大小关系:④>①>②>③ | |
| C. | 将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1 NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:c(HA)>c(Na+)>c(A-) | |
| D. | 物质的量浓度之比为1:1的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)═c(${HCO}_{3}^{-}$)+c(${CO}_{3}^{2-}$) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某无色稀溶液X中,可能含有表所列离子中的某几种.
某无色稀溶液X中,可能含有表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
| A. | 若Y是盐酸,则Oa段转化为沉淀的离子(表中,下同)只有AlO2- | |
| B. | 若Y是盐酸,则溶液中可能含有的阳离子是Al3+ | |
| C. | 若Y是NaOH溶液,则bc段反应的离子方程式为 Al(OH)3+OH-═AlO2-+2H2O | |
| D. | 若Y是NaOH溶液,则X溶液中只存四种离子是:Al3+、Fe3+、NH4+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CH3COOCH3+H2O.
CH3COOCH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酯存在于许多水果鲜花中具有特殊的香味 | |
| B. | 乙酸和甲醇在一定条件下也能发生酯化反应 | |
| C. | 酯化反应也属于取代反应 | |
| D. | 酯化反应中需要稀硫酸做催化剂 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上月考二化学试卷(解析版) 题型:选择题
某地甲、乙两工厂排放的污水中各含有下列8种离子中的4种(两厂废水所含离子不同):Ag+、Ba2+、Fe2+、Na+、Cl-、SO42-、NO3-、OH-。若两厂单独排放污水都会造成较严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便能变得无色澄清的只含硝酸钠的溶液而排放,污染程度大大降低。根据所给信息有以下几种说法,你认为正确的是( )
A.Na+和NO3-来自同一工厂 B.Cl-和Fe2+一定来自同一工厂
C.SO42-和Cl-来自同一工厂 D.Ag+和Na+可能来自同一工厂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com