
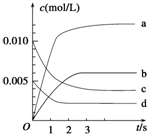
| A、AB的电离是吸热过程 |
| B、在35℃时,c(A+)>c(B-) |
| C、AB的电离程度(25℃)>(35℃) |
| D、c(A+)随温度升高而降低 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、向苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO
| ||
| B、用硫酸铜溶液除去乙炔中的硫化氢气体:Cu2++S2-=CuS↓ | ||
C、乙酸与碳酸钙溶液反应:2CH3COOH+CO
| ||
| D、酸性高锰酸钾溶液中通入乙炔后紫色褪去:2MnO4-+6H++C2H2=2Mn2++2CO2+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)△H<0体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
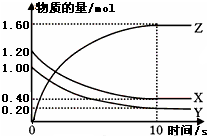 (1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则
(1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 物质转化关系 | a | b | c | d |
| A | 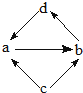 |
FeCl2 | FeCl3 | Fe | CuCl2 |
| B | NO | NO2 | N2 | HNO3 | |
| C | Na2CO3 | NaOH | Na2O2 | NaHCO3 | |
| D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使石蕊试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl-能大量共存 |
| B、含有大量AlO2-的溶液中:Na+、Ba2+、Cl-、HCO3- 能大量共存 |
| C、澄清透明的溶液中:Cu2+、Fe3+、NO3-、Cl-不能大量共存 |
| D、c(H+)=0.1mol?L-1的溶液中:Na+、Mg2+、SO42-、ClO-不能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验内容 | 实验方案或者目的 | |
| A | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将产生的气体通入溴的四氯化碳溶液 | 证明溴乙烷发生消去反应 |
| B | 向相同体积的甲苯和苯中加入3滴酸性KMnO4溶液振荡,观察现象 | 证明与苯环相连的甲基易被氧化 |
| C | 将装有NO2的玻璃球浸泡在冷、热水中,观察颜色变化 | 探究温度对化学平衡的影响 |
| D | 向碳酸钠固体中加入过量的盐酸,产生的气体通入硅酸钠溶液中,产生白色沉淀 | 证明碳酸的酸性比硅酸强 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、W、M的某种单质可作为水处理中的消毒剂 |
| B、电解YW2的熔融物可制得Y和W的单质 |
| C、相同条件下,W的氢化物水溶液酸性比Z弱 |
| D、X、M两种元素形成的一种化合物与水反应可生成M的某种单质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com