
在硫酸的制备中,最后的产品是98%的硫酸或20%的发烟硫酸(H2SO4和SO3的混合物,其中SO3的质量分数为20%)。
(1)若98%硫酸可表示为SO3·aH2O,20%的发烟硫酸可表示为SO3·bH2O,则a、b的值(a、b可用分数表示)分别是:a= ,b= 。
(2)用m(H2O)=k·n(SO3)分别表示SO3转化成上述两种硫酸时,所用水的质量与SO3的物质的量的关系式(即求k)分别是:
m1(H2O)= n1(SO3),m2(H2O)= n2(SO3)。
(3)若工厂同时生产上述两种硫酸,则上述两种硫酸的质量比x(W1为98%的硫酸的质量、W2为20%的发烟硫酸的质量)与SO3的用量的物质的量之比y的关系是 。
(1) ![]()
![]()
(2)20g·mol-1? 13.8g·mol-1
(3)y=0.938x
(1)“98%的硫酸”指100g硫酸溶液中有98gH2SO4、2gH2O。若用SO3·aH2O表示,则题意为1molSO3、amolH2O,因此,a=![]() 。
。
而对20%的发烟硫酸,100g中应有H2SO4 80g、SO3 20g。
(2)利用(1)中的结果可方便地求解k的值。
(3)分别求出两种浓度时,n(SO3)与W的关系,其比值中非![]() 的部分即为所求。
的部分即为所求。
解:(1)对98%的硫酸,有:
?a=![]() =
=![]()
而对20%的发烟硫酸,则有:
?b=![]() =
=![]()
(2)由a=![]() 可得:
可得:
?n1(H2O)=a·n1(SO3)
18g·mol-1×n1(H2O)=18g·mol-1×a×n1(SO3)=m1(H2O)
所以k=18g·mol-1×a=20g·mol-1
由b·n2(SO3)=n2(H2O)
18g·mol-1×n2(H2O)=18g·mol-1×b×n2(SO3)
m2(H2O)=18g·mol-1×b×n2(SO3)=18g·mol-1×![]() ×n2(SO3)
×n2(SO3)
所以k=![]() =13.8g·mol-1。
=13.8g·mol-1。
(3)设98%的硫酸所需SO3的用量为n1(SO3),20%的发烟硫酸所需SO3的用量为n2(SO3),则
?n1(SO3)=W1×![]() =
=![]()
?n2(SO3)=W2×![]() +W2×
+W2×![]() =
=![]()
两式相除得:
y=n1(SO3)∶n2(SO3)=0.938×![]() =0.938x。
=0.938x。


科目:高中化学 来源: 题型:阅读理解
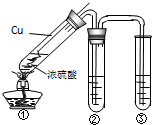 化学是一门以实验为基础的自然科学.
化学是一门以实验为基础的自然科学.查看答案和解析>>
科目:高中化学 来源:重难点手册 高中化学·必修1 配人教版新课标 人教版新课标 题型:043
| |||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)若98%硫酸可表示为SO3·aH2O,20%的发烟硫酸可表示为SO3·bH2O,则a、b的值(a、b可用分数表示)分别是:a= ,b= 。
(2)用m(H2O)=k·n(SO3)分别表示SO3转化成上述两种硫酸时,所用水的质量与SO3的物质的量的关系式(即求k)分别是:
m1(H2O)= n1(SO3),m2(H2O)= n2(SO3)。
(3)若工厂同时生产上述两种硫酸,则上述两种硫酸的质量比x(W1为98%的硫酸的质量、W2为20%的发烟硫酸的质量)与SO3的用量的物质的量之比y的关系是 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省济南市高一上学期期末考试化学试卷(带解析) 题型:填空题
(12分)化学是一门以实验为基础的自然科学。
(1)下列说法中,符合实验安全规范要求的是 (填序号字母)。
① 闻气体的气味时,应用手在瓶口轻轻煽动,使少量的气体飘进鼻孔
② 在实验室做铜和浓硝酸反应制备二氧化氮的实验时,应该在通风橱中进行
③做H2还原CuO实验时,先加热CuO至高温,然后立即通入H2使反应发生
④实验中当有少量的过氧化钠剩余时,用纸包裹好后将其放入垃圾桶中
(2)某学习小组用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应及部分产物的性质(装置中的铜丝可适当上下抽动)。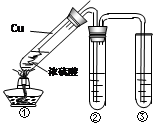
① 当反应进行一段时间后,欲使反应迅速停止,可采取的措施为 。
② 若装置②用来检验生成的气体产物的性质,在装置②的试管中加入的试剂为品红试液,通入气体后,现象为 ,此现象证明该气体产物具有 性。
③ 装置③中盛有某单质的水溶液,用来检验气体产物的还原性,则该单质的水溶液为
,反应的化学方程式为 。
④ 实验最后,要将图①大试管中的液体与水混合,以观察颜色检验存在的离子,从安全角度考虑,混合的方法应该是 。
⑤ 实验中,在所用仪器及仪器间连接都完好的情况下,同学们仍闻到了较强的刺激性气味,说明此实验的整套装置设计有缺陷,会造成空气污染。改进此实验装置的方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com