
已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,但存在溶解平衡。当达到平衡时,溶液中离子浓度的乘积是一个常数(此常数用Ksp表示,Ksp和水的Kw相似)。如
AgX(s) Ag+(aq)+X-(aq),Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
Ag+(aq)+X-(aq),Ksp(AgX)=c(Ag+)·c(X-)=1.8×10-10
AgY(s) Ag+(aq)+Y-(aq),Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
Ag+(aq)+Y-(aq),Ksp(AgY)=c(Ag+)·c(Y-)=1.0×10-12
AgZ(s) Ag+(aq)+Z-(aq),Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
Ag+(aq)+Z-(aq),Ksp(AgZ)=c(Ag+)·c(Z-)=8.7×10-17
下列说法错误的是( )
A.这三种物质在常温下溶解度最小的是AgZ
B.将AgY溶解于水后,向其中加入AgX,则c(Y-)减小
C.在25℃时,取0.188 g AgY(相对分子质量为188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中c(Y-)=1.0×10-4mol·L-1
D.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
科目:高中化学 来源: 题型:
电解装置如图所示。图中B装置盛1 L 2 mol·L-1的Na2SO4溶液,A装置中盛1 L 2
mol·L-1 AgNO3溶液。通电后,湿润的淀粉KI试纸的C端变蓝色。电解一段时间后,试回
答:
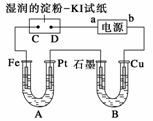
(1)A中发生反应的化学方程式为_________________________________________。
(2)在B中观察到的现象是_____________________________________________。
(3)室温下若从电解开始到时间t时,A、B装置中共收集到0.168 L(标准状况)气体。若电
解过程中无其他副反应发生,且溶液体积变化忽略不计,则在t时,A溶液中酸的浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
重庆汽车研究所国家燃气汽车工程技术研究中心经过多年攻关,早已完成了国内第一辆达到欧洲Ⅲ号排放标准的天然气单一燃料汽车的研制。时隔一年,在此基础上, 又一举拿下了汽油——天然气双燃料汽车,并且达到了欧洲Ⅲ号排放标准,得到了政府的大力支持并被推广使用。
又一举拿下了汽油——天然气双燃料汽车,并且达到了欧洲Ⅲ号排放标准,得到了政府的大力支持并被推广使用。
(1)天然气的主要成分为 ,是 在隔绝空气条件下,经微生物发酵作用形成的,因此,天然气中贮藏的化学能最终是来自于
(2)从石油中获得更多轻质燃油的方法是______________________。
(3)利用天然气可以制高档墨水和橡胶用的炭黑,同时得到合成氨工业所需H2,该反应的化学方程式为 ,天然气成分两分子偶联可以得到乙烯,在一定程度上缓解了石油危机,该反应的化学方程式为________________________________________________。
(4)政府推广使用燃气汽车的主要目的是 (填序号)。A.延长发动机使用寿命
B.促进西部经济发展
C.减少污染
D.提高能源利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,Ag2SO4、AgCl、AgI的溶度积常数依次为Ksp(Ag2SO4)=7.7×10-5、Ksp(AgCl)=1.8×10-10、Ksp(AgI)=8.3×10-17。下列有关说法中,错误的是( )
A.常温下,Ag2SO4、AgCl、AgI在水中的溶解能力依次减弱
B.在AgCl饱和溶液中加入NaI固体,有AgI沉淀生成
C.Ag2SO4、AgCl、AgI的溶度积常数之比等于它们饱和溶液的物质的量浓度之比
D.在Ag2SO4饱和溶液中加入Na2SO4固体有Ag2SO4沉淀析出
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA是阿伏加德罗常数的值,下列说法正确的是
A.1 L1mol·L-1的NaClO溶液中含有ClO-的数目为NA
B.60g 二氧化硅含有的共价键数为2NA
C.7.8g 钾与100mL 1mol·L-1盐酸充分反应生成气体分子数为0.1NA
D.标准状况下,7.1g 氯气与足量的石灰乳充分反应,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:①2CH3OH(1)+ 3O2(g)= 2CO2(g)+ 4H2O(g)ΔH1 = –1275.6 kJ·mol– 1
②2CO(g)+ O2(g)= 2CO2(g) ΔH2 = –566.0 kJ·mol– 1
③H2O(g)= H2O(1) ΔH3 = –44.0 kJ·mol– 1写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(2)生产甲醇的原料CO和H2来源于:CH4(g)+ H2O(g) CO(g)+ 3H2(g)
CO(g)+ 3H2(g)
① 一定条件下CH4的平衡转化率与温度、压强的关系如图a。则,Pl P2;A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为__________。(填“<”、“>”“=”)

② 100℃时,将1 mol CH4和2 mol H2O通入容积为100 L的反应室,反应达平衡的标志是: 。
a.容器内气体密度恒定
b.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
c.容器的压强恒定
d.3v正(CH4)= v逆(H2)如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K =
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为 。用该原电池做电源,常温下,用惰性电极电解200 mL饱和食盐水(足量),消耗的标准状况下的CO 224 mL,则溶液的pH = 。(不考虑溶液体积的变化)
(4)氢氧燃料电池的三大优点是: 、 、能连续工作。
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物G的合成路线如下:
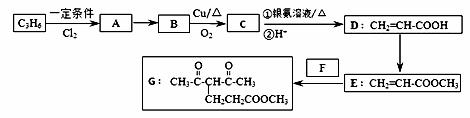
(1)D中含氧官能团的名称为 ,1 mol G发生加成反应最多消耗 mol H2 。
(2)除掉E中含有少量D的试剂和分离方法分别是 , ;
(3)下列说法正确的是 (填字母序号)。
a.A易溶于水
b.只用溴水即可确定C中含有碳碳双键
c.E经加聚、碱性条件下水解,所得高聚物可做具有高吸水性能的树脂
d.E是CH2=CHCOOCH2CH3的同系物
(4)写出A→B的化学反应方程式 ;
写出C和银氨溶液反应的离子方程式 。
(5)反应E + F→ G属于下列麦克尔加成反应类型,则F的结构简式为 。
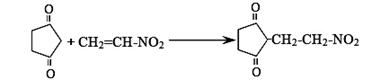

(6)比G少2个氢原子的物质具有下列性质:①遇FeCl3溶液显紫色;②苯环上的一氯取代物只有一种;③1mol物质最多可消耗2mol Na和1mol NaOH。任写一种该物质的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是元素周期表中原子序数依次增大的四种常见元素,只有W位于长周期。其相关信息如下表:
| 元素 | 相关信息 |
| X | X原子的电子层数是最外层电子数的2倍 |
| Y | Y与X同周期,该元素与氧能形成多种化合物 |
| Z | Z的基态原子的最高能级上有2个单电子,其最高价氧化物对应的水化物是一种强酸 |
| W | W是一种过渡金属元素,在潮湿的空气中其表面会生成一种绿色的化合物 |
(1)X的最高价氧化物对应的水化物的化学式为__________________________,预测该化合物________(填“难”或“易”)溶于水。
(2)Z位于元素周期表第______周期第_____族;W元素的基态原子的核外电子排布式为________________________________________________________。
(3)Y和Z的氢化物中,前者较稳定,则共价键的键长较长的物质是__________(填化学式)。
(4)Y、Z和氢元素组成的某种含氧酸正盐溶液中,Z呈现最高正价。该物质的水溶液呈酸性,其原因是___________________(填离子方程式)。
(5)W2Z能与Y的最高价氧化物对应的水化物的稀溶液反应,生成物中无难溶物,写出反应的化学方程式:________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com