
【题目】以乙炔与甲苯为主要原料,按下列路线合成一种香料W:
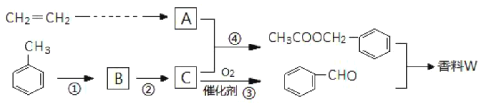
(1)写出实验室制备乙炔的化学方程式___________。
(2)反应①的反应试剂、条件是________,上述①~④反应中,属于取代反应的是________。
(3)写出反应③的化学方程式_____________。
(4)检验反应③是否发生的方法是_______。
(5)写出两种满足下列条件的![]() 同分异构体的结构简式______。
同分异构体的结构简式______。
a.能发生银镜反应 b.苯环上的一溴代物有两种
【答案】![]() 氯气、光照 ①②④
氯气、光照 ①②④ 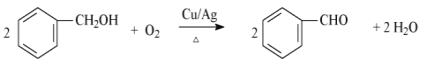 取样,滴加新制氢氧化铜悬浊液,加热煮沸,有砖红色沉淀生成,可证明反应③已经发生
取样,滴加新制氢氧化铜悬浊液,加热煮沸,有砖红色沉淀生成,可证明反应③已经发生 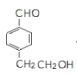 、
、 、
、
【解析】
由C的结构及反应④为酯化反应可知,A为CH3COOH,C为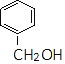 ,则反应①为与氯气光照下发生取代反应,生成B为
,则反应①为与氯气光照下发生取代反应,生成B为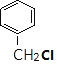 ,反应②为卤代烃的水解反应,反应③为醇的催化氧化反应,
,反应②为卤代烃的水解反应,反应③为醇的催化氧化反应,
(1)实验室用碳化钙和水反应制备乙炔,化学方程式![]() 。
。
答案为:![]() ;
;
(2)根据上述分析,反应①的反应试剂为氯气,条件是光照,上述①~④反应中,属于取代反应的是①②④,
故答案为:①②④;
(3)反应③为 与氧气在催化剂作用下发生氧化反应生成
与氧气在催化剂作用下发生氧化反应生成![]() ,化学方程式为
,化学方程式为
 。
。
答案为: ;
;
(4)检验反应③是否发生的方法是:取样,滴加新制氢氧化铜悬浊液,加热,有砖红色沉淀生成,可证明反应③已经发生,
故答案为:取样,滴加新制氢氧化铜悬浊液,加热,有砖红色沉淀生成,可证明反应③已经发生;
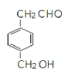
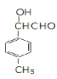
(5)![]() 的同分异构体满足a.能发生银镜反应,含CHO;b.苯环上的一溴代物有两种,苯环上有2种H,则2个取代基位于对位,符合条件的结构简式为
的同分异构体满足a.能发生银镜反应,含CHO;b.苯环上的一溴代物有两种,苯环上有2种H,则2个取代基位于对位,符合条件的结构简式为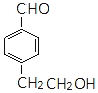 、
、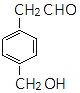 、
、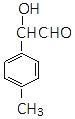 等,
等,
答案为: 、
、 、
、 。
。


科目:高中化学 来源: 题型:
【题目】某兴趣小组为探究SO2与Fe(NO3)3稀溶液反应的情况,实验装置如图:
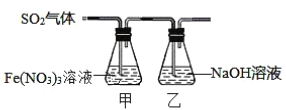
请回答:
(1)实验过程中,甲中溶液由黄色变为浅绿色但立即又变为黄色。请写出甲中溶液由浅绿色变为黄色的离子方程式___。
(2)请设计实验方案,检验反应后甲溶液中的金属阳离子___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂排放的工业废水中含Fe3+、Al3+、Cu2+,为了减少环境污染,变废为宝,利用废铁屑和其它化学试剂进行如下操作,得到了Fe2O3、Al2O3和金属Cu。
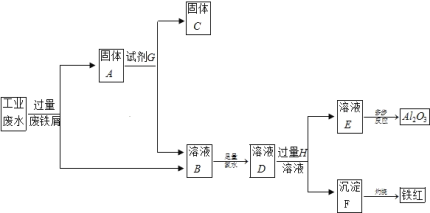
请回答:
(1)固体A的成分是____________(用化学式表示)。
(2)溶液B→沉淀F的现象是_______________,用化学方程式表示沉淀产生此现象的原理_______。
(3)写出下列反应的离子方程式:反应①中Fe3+发生的反应:_____________,D→E:__________。
(4)小明认为由溶液B→溶液D的过程并不符合绿色化学,所以将氯水换成了H2O2溶液,在该转化过程中若转移2mol 电子,则消耗质量分数为30%的H2O2溶液的质量为________g(精确到0.1g)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.乙醇、乙二醇、丙三醇互为同系物
B.1mol甲基![]() 所含的电子数约为10×6.02×
所含的电子数约为10×6.02×![]()
C.14g分子式为![]() 的链烃中含有的C=C的数目一定为
的链烃中含有的C=C的数目一定为![]()
D.同分异构体间具有完全相同的物理性质和化学性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机一无机活性材料的液流电池具有能量密度大、环境友好等特点。其负极反应为Zn-2e-+4NH3·H2O=Zn(NH3)42++4H2O,以LiPF6为电解质,工作示意图如图。电池放电过程中,下列说法错误的是
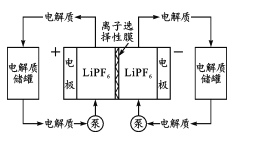
A.电子从负极经外电路流向正极
B.已知正极发生反应: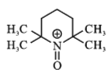 +e-→
+e-→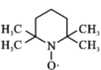 ,此过程为还原反应
,此过程为还原反应
C.负极附近溶液pH会降低
D.电解质溶液中的Li+自左向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯酚是一种很有价值的化工原料,年产量可达几百万吨。苯酚可合成著名的解热镇痛药——阿司匹林,也可合成聚碳酸酯,其合成路线如下:

(1)阿司匹林分子中的含氧官能团名称为_______;G的化学名称是____。
(2)E为饱和一元酮,其结构简式为________;H和K合成聚碳酸酯的反应类型是_____。
(3)鉴别G和阿司匹林的一种显色试剂为___________
(4)已知K的相对分子质量为99,其分子式为____________
(5)写出阿司匹林与足量NaOH溶液反应的化学方程式_________
(6)写出能同时满足以下条件的阿司匹林的两种异构体的结构简式_______________
①苯环上只有两种一氯代物;②含有羧基;③水解产生酚。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C分别是三种常见金属单质,其中B的氧化物和氢氧化物都是两性化合物。A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
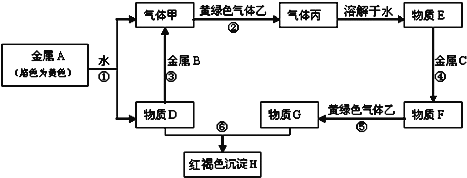
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:D_______,乙_____。
(2)在反应①-⑥中,不属于氧化还原反应的是__________。
(3)检验溶液G中阳离子的试剂为____________(填化学式),现象为_____________。
(4)写出下列反应的化学方程式:反应③:____________,气体乙与D物质溶液反应:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸合铁(Ⅲ)酸钾晶体{Ka[Fe(C2O4)b]·cH2O}易溶于水,难溶于乙醇,110 ℃可完全失去结晶水,是制备某些铁触媒的主要原料。实验室通过下列方法制备Ka[Fe(C2O4)b]·cH2O并测定其组成:
Ⅰ.草酸合铁酸钾晶体的制备
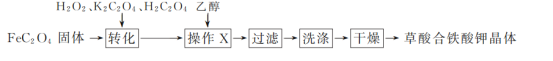
(1)“转化”过程中若条件控制不当,会发生H2O2氧化H2C2O4的副反应,写出该副反应的化学方程式:_________________________。
(2)“操作X”中加入乙醇的目的是_______________________。
Ⅱ. 草酸合铁酸钾组成的测定
步骤1:准确称取两份质量均为0.4910 g的草酸合铁酸钾样品。
步骤2:一份在N2氛围下保持110℃加热至恒重,称得残留固体质量为0.4370 g。
步骤3:另一份完全溶于水后,让其通过装有某阴离子交换树脂的交换柱,发生反应:aRCl+[Fe(C2O4)b]a-=Ra[Fe(C2O4)b]+aCl-,用蒸馏水冲洗交换柱,收集交换出的Cl-,以K2CrO4为指示剂,用0.1500 mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液20.00 mL。
(3)若步骤3中未用蒸馏水冲洗交换柱,则测得的样品中K+的物质的量________(填“偏大”“偏小”或“不变”)。
(4)通过计算确定草酸合铁酸钾样品的化学式(写出计算过程)。 ________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡元素参与组成的新型材料有着广泛的用途,回答下列问题。
(1)基态铁原子核外共有________种不同空间运动状态的电子。铁、钴、镍基态原子中,核外未成对电子数最少的原子价层电子轨道表示式(电子排布图)为________。
(2)NiO、FeO的晶体结构类型与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和74pm,则熔点NiO________FeO(填“>”“<”或“=”),原因是________。
(3)Cr的一种配合物结构如图所示:
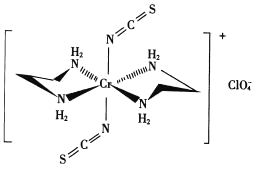
①阴离子![]() 的空间构型为________形。
的空间构型为________形。
②配离子中,中心离子的配位数为_______,N与中心原子形成的化学键称为_______键。
③配体H2NCH2CH2NH2(乙二胺)中碳原子的杂化方式是________,分子中三种元素电负性从大到小的顺序为________。
(4)一种新型材料的晶胞结构如图1所示,图2是晶胞中Sm和As原子的投影位置。
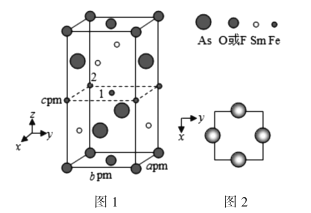
图1中F和O共同占据晶胞的上下底面位置,若两者的比例依次用x和1x代表,则该化合物的化学式表示为________,晶体密度ρ=________g·cm3(用含x的表达式表示,设阿伏加德罗常数的值为NA)。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标(![]() ),则原子2的坐标为________。
),则原子2的坐标为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com