
【题目】硫代硫酸钠可用作脱氯剂,已知25.0 mL 0.1 mol·L-1的Na2S2O3溶液恰好把标准状况下112 mL Cl2完全转化为Cl-时,S2![]() 转化成( )
转化成( )
A.S2-B.SC.![]() D.
D.![]()
科目:高中化学 来源: 题型:
【题目】实验室制备苯甲醇和苯甲酸的化学原理是
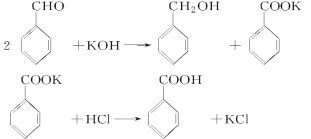
已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3 ℃;苯甲酸的熔点为121.7 ℃,沸点为249 ℃,溶解度为0.34 g;乙醚的沸点为34.8 ℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:
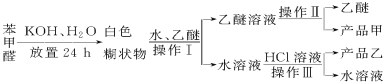
试根据上述信息回答下列问题:
(1)操作Ⅰ的名称是________,乙醚溶液中所溶解的主要成分是________。
(2)操作Ⅱ的名称是________,产品甲是________。
(3)操作Ⅲ的名称是________,产品乙是________。
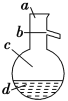
(4)如图所示,操作Ⅱ中温度计水银球上沿放置的位置应是________(填“a”“b”“c”或“d”),该操作中,除需蒸馏烧瓶、温度计外,还需要的玻璃仪器是__________________,收集产品甲的适宜温度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是人类利用最早的金属之一,其单质及化合物在人生产生活中有着广泛的应用。
(1)铜可以做成导线,Cu的焰色为___________色;基态Cu2+的核外电子占据的最高能层的能层符号为___________。
(2)铜可以作为乙醇和氧气反应的催化剂,2CH3CH2OH + O2![]() CH3CHO + 2H2O。写出与水具有相同空间构型的一个分子和一个离子______________(微粒由短周期元素组成)。从原子轨道重叠方式来看CH3CHO中所含的共价键类型有____________________,碳的杂化方式是______________。
CH3CHO + 2H2O。写出与水具有相同空间构型的一个分子和一个离子______________(微粒由短周期元素组成)。从原子轨道重叠方式来看CH3CHO中所含的共价键类型有____________________,碳的杂化方式是______________。
(3)高温超导是世界上最前沿的研究之一,如下图是第一个被发现的高温超导体氧化物的晶胞。该化合物的化学式为___________。与Cu2+紧邻的O2-的个数为___________。已知,阿伏加德罗常数为NA,则晶胞密度为___________g·cm-3。
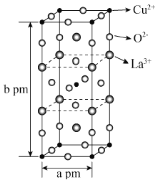
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年11月4日是《巴黎协定》气候协议生效的日期,其宗旨是提高绿色低碳转型的竞争力、抵御气候变化,人们需要用不同的方法将CO2进行转化利用。
(1)处理CO2的方法之一是使其与氢气反应合成甲醇。已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2(g)=2H2O(1) △H=-283.0kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(1) △H=-726.0kJ·mol-1
写出二氧化碳与氢气合成甲醇液体的热化学方程式_________;
(2)CO2经催化加氢还可合成低碳烯烃:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) △H=QkJ·mol-1在0.1MPa时,按n(CO2):n(H2)=1:3投料,右图表示平衡时四种气态物质的物质的量(n)与温度(T)的关系。
C2H4(g)+4H2O(g) △H=QkJ·mol-1在0.1MPa时,按n(CO2):n(H2)=1:3投料,右图表示平衡时四种气态物质的物质的量(n)与温度(T)的关系。
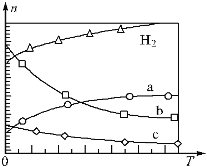
①Q______0(填“>”、“=”或“<”);
②曲线b表示的物质为_____。
(3)在强酸性的电解质水溶液中,用惰性材料做电极,电解CO2可得到多种燃料,其原理如右图所示。

①该工艺中能量转化方式主要有______;
②电解时,生成丙烯(C3H6)的电极反应式为______。
(4)以CO2为原料制取碳(C)的太阳能工艺如右图所示。

①过程1中发生反应的化学方程式为______;
②过程2中每生成1molFe3O4[FeOFe2O3]转移电子的物质的量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,W的单质为常见的半导体材料,X、W为同一主族元素。X、Z、W分别与Y形成的最高价化合物为甲、乙、丙。结合如图转化关系,下列判断正确的是( )
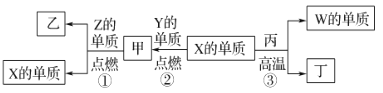
A.X的氢化物沸点低于Y的氢化物沸点
B.W的单质可以用作计算机芯片,太阳能电池,丙是玛瑙的主要成分
C.甲、丙、丁均为酸性化合物
D.工业上用X的单质和乙来制取Z单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
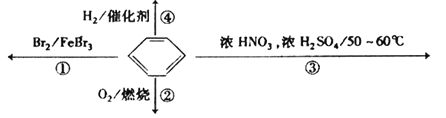
A. 反应![]() 为取代反应,有机产物的密度比水小
为取代反应,有机产物的密度比水小
B. 反应![]() 为取代反应,有机产物是一种烃
为取代反应,有机产物是一种烃
C. 反应![]() 中1mol苯最多与
中1mol苯最多与![]() 发生加成反应,是因为苯分子含有三个碳碳双键
发生加成反应,是因为苯分子含有三个碳碳双键
D. 反应![]() 为氧化反应,反应现象是火焰明亮并带有较多的黑烟
为氧化反应,反应现象是火焰明亮并带有较多的黑烟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯与溴反应的实验装置如下图所示:
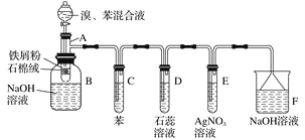
其中A为具有支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量的铁屑粉。请回答下列问题:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中发生反应的化学方程式(有机物写结构简式)___________________________________________________。
(2)试管C中苯的作用是__________________________________________________________。
(3)反应开始后,观察D和E两试管,看到的现象是__________________________________________________。
(4)反应2 min~3 min后,在B中的氢氧化钠溶液里可观察到的现象是___________________。
(5)在上述整套装置中,具有防倒吸作用的仪器有___________________________________。
(6)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这三个优点外,还有一个优点是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是 ( )
A. 稀硫酸滴在铁片上:2Fe+6H+===2Fe3++3H2↑
B. 碳酸氢钠溶液与稀盐酸混合:HCO3-+H+=H2O+CO2↑
C. 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-===Cu(OH)2↓+![]()
D. 硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-===AgCl↓+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的氢氧化钠溶液,测得生成的气体(标准状况,下同)体积为b L,样品中铝的质量是______________g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是:_______________________,氧化铁与铝的质量比是_____________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c:b__________。
(4)用铝热法还原下列物质,制得金属各1mol,消耗铝最少的是____________
A.MnO2 B.Fe3O4 C.Cr2O3 D. V2O5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com