
 验证NH4Cl晶体中含有NH4+.将少量晶体于两端开口的硬质玻璃管中加热,如图所示.
验证NH4Cl晶体中含有NH4+.将少量晶体于两端开口的硬质玻璃管中加热,如图所示.分析 氯化铵分解生成氨气和氯化氢,氨气的密度比空气小,可在a处检验氨气,以此解答该题.
解答 解:(1)氯化铵分解生成氨气和氯化氢,方程式可为NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+HCl↑,故答案为:NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+HCl↑;
(2)氨气的密度比空气小,可在a处检验氨气,可用红色石蕊试纸检验,试纸变为蓝色,故答案为:a;红色石蕊; 试纸变蓝.
点评 本题考查氯化铵以及氨气的性质,为高频考点,侧重于学生的分析、实验能力的考查,注意把握氨气与氯化氢的密度大小,为该题的易错点,难度不大.


科目:高中化学 来源: 题型:选择题
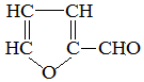 ),糠醛是重要的化工原料,用途广泛.关于糠醛的说法,不正确的是( )
),糠醛是重要的化工原料,用途广泛.关于糠醛的说法,不正确的是( )| A. | 其核磁共振氢谱有3种不同类型的吸收峰 | |
| B. | 1 mol糠醛可与3 mol H2 发生加成反应 | |
| C. | 可与新制的Cu(OH)2浊液在加热时反应生成红色沉淀 | |
| D. | 与苯酚在一定条件下反应得到结构简式为 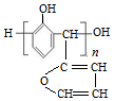 的产物 的产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向CaCl2溶液中通入SO2气体 | B. | 向Ba(OH)2溶液中通入过量CO2气体 | ||
| C. | 向FeCl2溶液中加入过量NaOH溶液 | D. | 向Al2(SO4)3溶液中加入过量NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸具有脱水性,因而能使蔗糖炭化 | |
| B. | 浓硫酸有强氧化性,不可贮存在铝、铁容器中 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| D. | 稀释浓硫酸时,应将水沿着器壁慢慢加入到浓硫酸中,并用玻璃棒不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:Na2CO3<NaHCO3 | |
| B. | 相同温度下,在水中的溶解度:Na2CO3<NaHCO3 | |
| C. | 等质量的Na2CO3和NaHCO3最多产生CO2的量:Na2CO3<NaHCO3 | |
| D. | 等物质的量的Na2CO3和NaHCO3最多消耗盐酸的量:Na2CO3<NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向容量瓶转移液体时,玻璃棒下端伸入到容量瓶刻度线以下 | |
| B. | 用玻璃棒蘸取CH3COOH溶液点在已湿润的pH试纸上,测定该溶液的pH | |
| C. | 用长颈漏斗分离出乙酸与乙醇反应的产物 | |
| D. | 测定中和热的实验中,应将酸、碱溶液一次性倒入量热装置中,并不断搅拌,待温度 稳定后记下温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
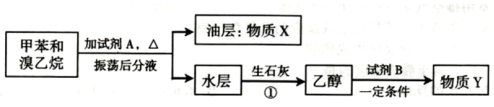
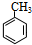 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  将NO2球浸泡在冷水中和热水中 | |||||||||||||
| B. | 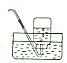 排饱和食盐水收集氯气 | |||||||||||||
| C. | 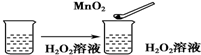 | |||||||||||||
| D. |
| |||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com