
分析 (1)水溶液中电离出的阳离子全部是氢离子的化合物为酸,水溶液中电离出的阴离子全部是氢氧根离子的化合物为碱,金属阳离子和酸根阴离子构成的化合物为盐,两种元素组成,其中一种为氧元素的化合物为氧化物,据此分析判断;
(2)根据电解质的定义分析,在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;非电解质是在水溶液里和熔融状态下都不能导电的化合物,包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等);
(3)根据物质导电的原因分析,只要含有自由移动的离子或自由电子即可.
解答 解:①Mg是金属单质,有自由移动的电子,能够导电,既不是电解质也不是非电解质,属于金属单质;
②液态氯化氢只存在氯化氢分子不能导电,其水溶液能电离出氢离子和氯离子导电,为电解质属于酸;
③干冰为CO2只存在分子,没有自由移动的离子,所以不能导电;二氧化碳在水溶液中与水反应生成碳酸,碳酸电离出自由移动的离子导电,二氧化碳自身不能电离,二氧化碳是非电解质;
④BaSO4没有自由移动的离子不导电; 虽然硫酸钡在水中的溶解度很小,但硫酸钡只要溶解就完全电离且在熔融状态下能够完全电离,所以硫酸钡是电解质属于盐;
⑤单质碘不能导电,既不是电解质也不是非电解质,属于非金属单质;
⑥熔融氢氧化钠电离出自由移动的钠离子和氢氧根离子,能导电;它是化合物中的碱,属于电解质;
⑦稀硫酸有自由移动的氢离子和硫酸根离子,能导电,但稀硫酸为硫酸溶液,是混合物,所以,它既不是电解质也不是非电解质;
⑧乙醇是化合物,但其水溶液只存在乙醇分子,不导电,属于非电解质;
(1)属于酸的是 ②液态氯化氢;属于碱的是⑥熔融氢氧化钠;属于盐的是④BaSO4;属于氧化物的是③干冰,
故答案为:②;⑥;④;③;
(2)电解质包括酸、碱、盐、活泼金属氧化物和水,所以②④⑥符合,非电解质包括一些非金属氧化物、氨气、大多数有机物(如蔗糖、酒精等),所以③⑧是非电解质;
故答案为:②④⑥;③⑧;
(3)①有自由电子,所以能导电;⑥有自由移动的离子,所以能导电;⑦有自由移动的离子,所以能导电,
故答案为:①⑥⑦.
点评 本题考查了物质分类、物质组成、电解质溶液导电的原因及电解质、非电解质的定义,物质导电的原因只要含有自由移动的离子或自由电子即可,题目难度不大.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吗啡 | B. | 可卡因 | C. | 甘油 | D. | 海洛因 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化镁和稀盐酸反应 | B. | Ba(OH)2溶液滴入稀硫酸中 | ||
| C. | 澄清石灰水和稀硝酸反应 | D. | CH3COOH溶液和NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
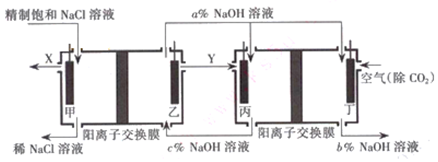
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 镁、铝、铁是重要的金属,在工业生产中用途广泛.
镁、铝、铁是重要的金属,在工业生产中用途广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
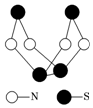 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质的分子式为SN | |
| B. | 该物质的分子中只含共价键 | |
| C. | 该物质具有很高的熔、沸点 | |
| D. | 该物质与化合物S2N2互为同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com