
 3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价 (填“升高”或“降低”),氮元素被 (填“氧化”或“还原”,下同),稀硝酸的作用是 、 .在该反应中,若消耗了32g铜,则转移电子数目为 mol.
3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价 (填“升高”或“降低”),氮元素被 (填“氧化”或“还原”,下同),稀硝酸的作用是 、 .在该反应中,若消耗了32g铜,则转移电子数目为 mol. 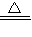 3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价升高;氮元素化合价从+5价变化为+2价,化合价降低做氧化剂被还原发生还原反应;硝酸在反应前后生成一氧化氮气体的做氧化剂,生成硝酸铜的硝酸化合价未变化,做酸; 反应中若消耗了32g铜物质的量为0.5mol,则转移电子数目为1mol,
3Cu(NO3)2+2NO↑+4H2O,其中铜元素的化合价升高;氮元素化合价从+5价变化为+2价,化合价降低做氧化剂被还原发生还原反应;硝酸在反应前后生成一氧化氮气体的做氧化剂,生成硝酸铜的硝酸化合价未变化,做酸; 反应中若消耗了32g铜物质的量为0.5mol,则转移电子数目为1mol,

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)工业上用碳在高温下与二氧化硅反应制取粗硅。反应的化学方程式为:
SiO2+2CSi+2CO↑,在该反应中氧化剂是_____________________________,被氧化
的物质与被还原的物质的物质的量之比是____________________________。
(2)请写出铜和稀硝酸反应的化学方程式: ,若制得标准状况下的气体 4.48L,则参加反应的硝酸的物质的量为________ mol,转移电子的物质的量为________ mol.
查看答案和解析>>
科目:高中化学 来源:2011-2012学年沈阳铁路实验中学高二假期验收化学试卷 题型:填空题
(1)工业上用碳在高温下与二氧化硅反应制取粗硅。反应的化学方程式为:
SiO2+2C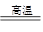 Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化
Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化
的物质与被还原的物质的物质的量之比是____________________________。
(2)请写出铜和稀硝酸反应的化学方程式: ,若制得标准状况下的气体 4.48L,则参加反应的硝酸的物质的量为________ mol,转移电子的物质的量为________ mol.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省嘉兴市高三上学期基础测试化学试卷(解析版) 题型:填空题
写出符合要求的化学方程式或离子方程式:
(1)铜和稀硝酸反应的化学方程式 。
(2)实验室用二氧化锰和浓盐酸制备氯气的离子方程式 。
(3)HCOOH和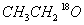 在一定条件下生成酯的化学方程式(标明
在一定条件下生成酯的化学方程式(标明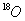 的位置) 。
的位置) 。
查看答案和解析>>
科目:高中化学 来源:2013届沈阳铁路实验中学高二假期验收化学试卷 题型:填空题
(1)工业上用碳在高温下与二氧化硅反应制取粗硅。反应的化学方程式为:
SiO2+2C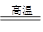 Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化
Si+2CO↑,在该反应中氧化剂是_____________________________,被氧化
的物质与被还原的物质的物质的量之比是____________________________。
(2)请写出铜和稀硝酸反应的化学方程式: ,若制得标准状况下的气体 4.48L,则参加反应的硝酸的物质的量为________ mol,转移电子的物质的量为________ mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com