
| A、干冰升华 |
| B、CaCO3(s)分解为CaO(s)和CO2(g) |
| C、NH3(g)与HCl(g)反应生成NH4Cl(s) |
| D、氯化钠溶于水中 |


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
| A、氧化性:Fe3+>Br2>I2>Fe(CN)63- |
| B、还原性:Fe(CN)64->I->Fe2+>Br- |
| C、氧化性:Br2>Fe3+>I2>Fe(CN)63- |
| D、还原性:Fe(CN)64->Fe2+>I->Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石灰石与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氧化铁和稀硫酸反应:O2-+2H+=H2O |
| C、向NaHSO4溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、向NaHCO3溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++CO32-=BaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )
HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )| A、HA是一种强酸 |
| B、x点,[A-]=[B-] |
| C、HB是一种弱酸 |
| D、原溶液中HA的物质的量浓度为HB的10倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热的纯碱溶液和冷的纯碱溶液洗涤油污效果一样好 |
| B、常温下,将氨水加入到盐酸中,所得溶液中一定存在:c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
| C、中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D、强电解质的水溶液的导电性一定比弱电解质的水溶液强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
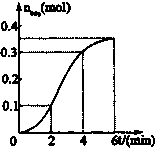 已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )| A、反应开始后2~4分钟内平均反应速率最大 |
| B、反应刚开始时反应速率较小,然后逐渐增大 |
| C、反应前阶段速率逐渐增大,是因为反应放热,使反应速率加快 |
| D、生成物CaCl2、CO2和H2O的总能量比反应物CaCO3和盐酸的总能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 条件① |
| 条件② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、右边加0.45g Al |
| B、左边加0.98g Mg |
| C、左边加14.4g Mg,右边加15.3g Al |
| D、左边加14.4g Mg,右边加14.85g Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com