
| A. | 总物质的量一定时,任意比混合,生成H2O的物质的量不同 | |
| B. | 总质量一定时,任意比混合,生成H2O的质量相同 | |
| C. | 总物质的量一定时,任意比混合,耗氧量相同 | |
| D. | 总质量一定时,任意比混合,耗氧量相同 |
分析 A、甲苯的分子式为C7H8,甘油的分子式为C3H8O3,两者中氢原子个数相同;
B、甲苯和甘油中的氢元素的百分含量均相同;
C、1mol甲苯燃烧消耗9mol氧气,1mol甘油燃烧消耗3.5mol氧气;
D、1mol甲苯即92g甲苯燃烧消耗9mol氧气,1mol甘油即92g甘油燃烧消耗3.5mol氧气,据此分析.
解答 解:A、甲苯的分子式为C7H8,甘油的分子式为C3H8O3,两者中氢原子个数相同均为8个,故只要混合物的总物质的量一定,无论两者所占的比例如何,生成的水的物质的量为定值,故A错误;
B、甲苯和甘油中的氢元素的百分含量均为ω%=$\frac{8}{92}$×100%=$\frac{2}{23}$×100%,故只要混合物的总质量一定,无论两者所占的比例如何,混合物所生成的水的质量为定值,故B正确;
C、1mol甲苯燃烧消耗9mol氧气,而1mol甘油燃烧消耗3.5mol氧气,当总物质的量一定时,若甲苯所占的比例大,则耗氧高,若甘油的所占的比例大,则混合物的耗氧量低,即混合物的耗氧量与甲苯和甘油所占的比例有关,不是定值,故C错误;
D、1mol甲苯即92g甲苯燃烧消耗9mol氧气,1mol甘油即92g甘油燃烧消耗3.5mol氧气,故当总质量一定时,甲苯的含量高,则耗氧量高,甘油的含量低,则耗氧量低,即混合物的含氧量与两者的含量有关,不是定值,故D错误.
故选B.
点评 本题考查了混合物在一定物质的量和一定质量时的耗氧量和生成物量的考查,应注意的是甲苯和甘油中氢原子个数、相对分子质量和氢元素的百分含量相同,同时,在审题时应注意看清题目所给的信息.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 苯(硝基苯):加少量蒸馏水振荡,静置分层后分液 | |
| B. | 乙醇(水):加新制的生石灰,蒸馏 | |
| C. | CO2(HCl、水蒸气):通过盛有碱石灰的干燥管 | |
| D. | 环己烷(苯):通入氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
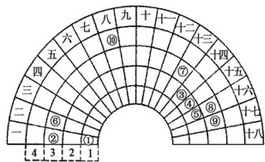 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,请回答下列问题
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,请回答下列问题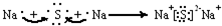
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③①⑤ | B. | ②③⑤① | C. | ④⑥③① | D. | ③⑥⑤① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
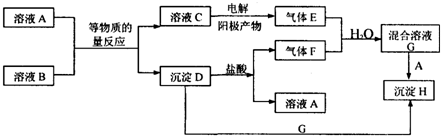
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe3+ | 2.1 | 3.2 |
| Al3+ | 4.1 | 5.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
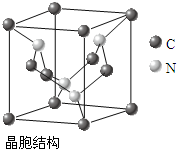
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| B. | 反应物总能量小于生成物总能量 | |
| C. | 升高温度,反应速率加快,但反应的△H不变 | |
| D. | 若在原电池中进行,反应放出的热量不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com