
| A. | Fe2+、NO3-、K+、Cl- | B. | K+、Al3+、HCO3-、Cl- | ||
| C. | H+、Ca2+、HCO3-、Cl- | D. | Ca2+、HCO3-、OH-、NO3- |
分析 A.四种离子之间不反应,能够共存;
B.铝离子与碳酸氢根离子发生双水解反应生成氢氧化铝沉淀和二氧化碳气体;
C.四种离子之间能够生成气体,不会生成沉淀;
D.四种离子之间反应能够生成沉淀,但不会生成气体.
解答 解:A.Fe2+、NO3-、K+、Cl-之间不反应,能够大量共存,故A不选;
B.Al3+、HCO3-之间反应生成氢氧化铝沉淀和二氧化碳气体,在溶液中不能大量共存,满足条件,故B选;
C.H+、HCO3-之间反应生成二氧化碳气体,但是没有沉淀生成,不满足条件,故C不选;
D.Ca2+、HCO3-、OH之间反应能够生成碳酸钙沉淀,但没有气体生成,不满足条件,故D不选;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:选择题
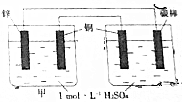
| A. | 乙池中铜电极反应是4OH--4e-═O2↑+2H2O | |
| B. | 甲池中的铜电极反应是2H++2e-═H2↑ | |
| C. | 碳棒上开始H+放电,然后是Cu2+放电 | |
| D. | 反应一段时间后甲乙两池溶液中H+的离子浓度不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碳酸氢钠溶液中滴加氢氧化钠溶液:OH-+HCO3-═CO32-+H2O | |
| B. | 溴化亚铁溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+2Cl- | |
| C. | 工业上将硫酸工业尾气SO2持续通入氨水中SO2+OH-═HSO3- | |
| D. | 向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无法计算 | B. | (m-0.8)g | C. | (m-1.2)g | D. | (m-1.6)g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1 mol•L-1 NH4Cl溶液的pH=1 | |
| B. | 工业上电解饱和食盐水时,以石墨为阴极,铁棒为阳极 | |
| C. | 反应CO2(g)+C(s)═2CO(g)在高温下可自发进行,则该反应的△H>0 | |
| D. | 常温下,在AgCl悬浊液中加入少量NaCl饱和溶液,[Ag+]减小,Ksp(AgCl)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6gFe在氧气中燃烧,完全反应时转移电子数为0.3NA | |
| B. | 标准状况下,4.48LCH3C1中所含原子数为NA | |
| C. | 1LpH=1的H2SO4溶液中含有的H+数为0.2NA | |
| D. | 常温下,1.7gNH3和3.65gHCl混合后,气体分子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2 NA | |
| B. | 0.1 mol/L (NH4)2SO4溶液与0.2 mol/L NH4Cl溶液中的NH4+数目相同 | |
| C. | 标准状况下,H2和CO混合气体8.96 L在足量O2中充分燃烧消耗O2分子数为0.2 NA | |
| D. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com