
| 1 |
| 2 |
| 1 |
| 2 |
| 0.02mol/L | ||
0.02mol/L��
|
| 1 |
| 2 |
| 1.08��10-10 |
| 10-3 |


 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��10 L 0.05 mol?L-1Ba��OH��2��Һ��20 L 0.05 mol?L-1 HNO3��Ӧʱ�ķ�Ӧ�����к��� |
| B��1 mol HCl����ͨ��1 L 0.01 mol?L-1 NaOH��Һ�з�Ӧʱ�ķ�Ӧ�����к��� |
| C��1 mol HClO��2 mol NaOH��Һ��Ӧʱ�ķ�Ӧ��Ҳ�������к��� |
| D��ֻҪǿ����ǿ����ϡ��Һ�з�Ӧ����1 molˮʱ�ķ�Ӧ�Ⱦ����к��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������N2��C2H4 |
| B��ƽ����Է�������Ϊ31��02��N2 |
| C���������C0��CH4 |
| D���������N2��02 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���٢� | C���ڢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
12 6 |
13 6 |
 ��
��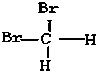 E�������Ǻ��� F����CH3��2CH2��C��CH3��4
E�������Ǻ��� F����CH3��2CH2��C��CH3��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����С�մ�����θ����ࣺHCO3-+H+�TCO2��+H2O |
| B�������ռ���Һ��2Al+2OH-+2H2O=AlO2-+3H2�� |
| C��FeͶ�������У�2Fe+6H+=2Fe3++3H2�� |
| D���Ȼ�����Һ�м��˹����İ�ˮ��Al3++3NH3?H2O�TAl��OH��3��+3NH4+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com