

| A. | 只有③ | B. | ②③ | C. | ①③⑤ | D. | ②③④ |
分析 根据同分异构体的定义判断,同分异构体是分子式相同结构式不同的化合物;单烯烃不能含有碳环.
解答 解:①立方烷、棱晶烷、金刚烷含有碳环,烷烃没有碳环,与烷烃分子式不同,故①错误;
②盆烯中含有一个碳碳双键,具有单烯烃的性质,能与溴水发生加成反应,故②正确;
③棱晶烷、盆烯、苯分子式相同,而结构不同,互为同分异构体,故③正确;
④④立方烷的二氯代物有3种同分异构体,分别处于邻边、面对角线和体对角线,故④正确;
⑤金刚烷的分子式为C10H16,癸炔的分子式为C10H18,不是同分异构体,故⑤错误;
故选D.
点评 本题考查烯烃的性质,同分异构体和同系物的区别,难度中等,注意根据题目所给信息解题.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.25mol/L | B. | 2mol/L | C. | 4mol/L | D. | 0.6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
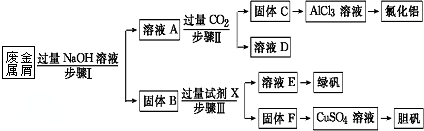
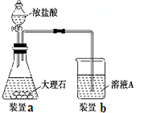 一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少.为了避免固体C减少,可采取的改进措施是在装置I和Ⅱ之间增加一个盛有饱和NaHCO3溶液的洗气瓶
一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少.为了避免固体C减少,可采取的改进措施是在装置I和Ⅱ之间增加一个盛有饱和NaHCO3溶液的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg、Ag | B. | Fe、Zn | C. | Al、Fe | D. | Mg、Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液:HCO3-+H2O?CO32-+H3O+ | |
| B. | NaHS溶液:HS-+H2O?H2S+OH- | |
| C. | Na2CO3溶液:CO32-+2H2O?H2CO3+2OH- | |
| D. | NH4Cl溶于D2O中:NH4++D2O?NH3•D2O+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol | B. | 0.5 mol | C. | 0.56 mol | D. | 0.4 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com