
| A. | 氯化铝 | B. | 碳酸氢钠 | C. | 硫酸镁 | D. | 高锰酸钾 |
分析 物质的溶液在蒸发皿中加热蒸干并灼烧,最后得到该物质固体,如果是盐,说明该物质为难挥发性酸的盐,且该盐较稳定,受热不易发生反应,据此分析解答.
解答 解:A.氯化铝易水解生成氢氧化铝和HCl,升高温度HCl易挥发,蒸干溶液得到的固体是氢氧化铝,灼烧氢氧化铝,氢氧化铝分解生成氧化铝,所以最终得到的固体是氧化铝,故A不选;
B.碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,故B不选;
C.形成硫酸镁的酸是硫酸,硫酸属于难挥发性酸,且硫酸镁较稳定,受热不发生反应,所以加热蒸干灼烧硫酸镁溶液最后得到的仍然是硫酸镁,故C选;
D.高锰酸钾不稳定,受热易分解生成锰酸钾、二氧化锰和氧气,所以得不到原来物质,故D不选;
故选C.
点评 本题考查盐类水解的应用,侧重考查物质性质,加热蒸干灼烧易挥发性酸的盐最终得到的物质是金属氧化物,加热蒸干灼烧难挥发性酸的盐且该盐不易发生反应时得到其物质本身.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{22.4an}{m{N}_{A}}$ L | B. | $\frac{22.4am}{n{N}_{A}}$ L | C. | $\frac{n{N}_{A}}{22.4ma}$ L | D. | $\frac{na}{22.4m{N}_{A}}$L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=6的降雨是酸雨 | |
| B. | 氯气泄漏后应顺风向低处跑 | |
| C. | 金属钠着火应用泡沫灭火器灭火 | |
| D. | SO2、NO2、可吸入颗粒物等过量排放导致雾霾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠投入水中立即熔化成闪亮的小球,说明反应放热且钠的熔点低 | |
| B. | 钠在空气中燃烧生成淡黄色的Na2O2 | |
| C. | 金属钠可以将铜从其盐溶液中置换出来 | |
| D. | 实验后剩余的钠块能放回原试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
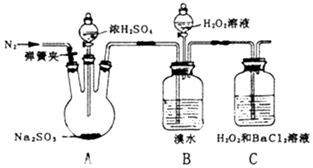 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).| 实验操作 | 实验现象 |
| i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
| iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化,继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化 | B. | 还原 | C. | 催化 | D. | 提供能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 放电时,Li+在电解质中由正极向负极迁移 | |
| B. | 放电时,负极的电极反应式为LixC6-xe-═xLi++C6 | |
| C. | 充电时,若转移1mole-,石墨C6电极将增重7xg | |
| D. | 充电时,阳极的电极反应式为LiCoO2-xe-═Li1-xCoO2+xLi+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用NH3•H2O溶液做导电性实验,灯泡很暗,说明NH3•H2O是弱电解质 | |
| B. | 等体积的pH都为3的酸HA和HB分别与足量的Mg反应,HA放出的H2多,说明酸性:HA>HB | |
| C. | 常温下,弱酸酸式盐NaHA溶液的pH=6,说明HA?的电离程度大于其水解程度 | |
| D. | pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com