
| A、硅胶的主要成分是硅酸钠 |
| B、明矾和氯化铁都可作净水剂 |
| C、发酵粉的主要成分是碳酸钠 |
| D、光导纤维的主要材料是晶体硅 |


科目:高中化学 来源: 题型:
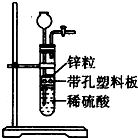 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )| A、①②③ | B、②④⑤ |
| C、①②④⑥ | D、②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
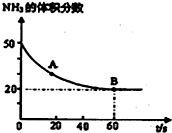 氮的化合物是一把双刃剑,它既是一种资源,又会给环境造成危害.
氮的化合物是一把双刃剑,它既是一种资源,又会给环境造成危害.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化铝的熔点很高,可用于制作耐高温材料 |
| B、在海轮外壳上镶人锌块,可减缓船体的腐蚀速率 |
| C、电解氯化镁饱和溶液,可制得金属镁 |
| D、明矾水解形成的胶体能吸附水中悬浮物,可用于水的净化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镁在空气中或纯净氧气中燃烧的产物都只有MgO |
| B、钠在敞口容器中存放或在空气中燃烧的产物都是Na2O2 |
| C、将四氧化三铁溶解于过量的硝酸,所得溶液中含有Fe3+、Fe2+ |
| D、偏铝酸钠和少量的二氧化碳反应一定得到Al(OH)3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅可以用做制造变压器铁芯的材料 |
| B、二氧化硅可用于制造光导纤维 |
| C、水玻璃可以用作木材防火剂 |
| D、石墨可用作绝缘材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打用于治疗胃溃疡病人的胃酸过多症 |
| B、工厂常用的静电除尘方法与胶体性质无关 |
| C、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板 |
| D、电解从海水中得到的氯化钠溶液可获得金属钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com