
| A. | 炭炉边放壶水,不能防止煤气中毒 | |
| B. | “水滴石穿”涉及学变化 | |
| C. | 颇受青眯的页岩气是非常规天然气,主要成分为CH4 | |
| D. | 油脂是高能量营养物质,肥胖者不能食用 |
分析 A.一氧化碳不溶于水;
B.水滴石穿中,石头的成分中含CaCO3,空气中含CO2,它们会发生反应:CaCO3+CO2+H2O═Ca(HCO3)2生成溶于水的Ca(HCO3)2,
C.页岩气主要成分是甲烷;
D.过多食用油脂使人发胖,应合理食用油脂.
解答 解:A.一氧化碳不溶于水,炭炉边放壶水,不能防止煤气中毒,故A正确;
B.水滴石穿中,石头的成分中含CaCO3,空气中含CO2,它们会发生反应:CaCO3+CO2+H2O═Ca(HCO3)2生成溶于水的Ca(HCO3)2,属于化学变化,故B正确;
C.页岩气是非常规天然气,主要成分为CH4,故C正确;
D.过多食用油脂使人发胖,应合理食用油脂,故D错误;
故选:A.
点评 本题考查了常见的化学知识,熟悉相关物质的性质是解题关键,题目难度不大.


 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO3和NH4NO3 | B. | NaOH和KCl | C. | NaN3和CaO2 | D. | AlCl3和MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性逐渐增强 | |
| B. | 化合价逐渐升高 | |
| C. | 失电子能力逐渐减弱 | |
| D. | 最高价氧化物对应的水化物碱性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 天津港爆炸案中对剧毒的氯化钠(NaCN)喷洒双氧水消毒,是利用了双氧水的氧化性 | |
| B. | 碳酸钙分解、氢氧化钡晶体和氧化铵固体反应,高温下铝与氧化铁反应都是吸热反应 | |
| C. | 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 | |
| D. | 屠呦呦女士利用乙醚萃取青蒿素获得了2015年度诺贝尔生理学或医学奖,为人类防治疟疾作出了重大贡献 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
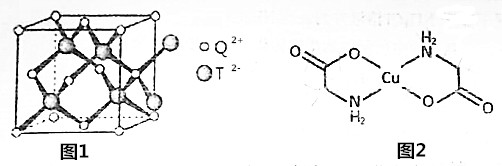
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2mL | 20 | / |
| Ⅱ | 2mL | 30 | / |
| Ⅲ | 1mL | 20 | 1mL蒸馏水 |
| Ⅳ | A | 20 | B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若HnXOm为强酸,则X的氢化物溶于水一定显酸性 | |
| B. | 若X(OH)n为强碱,则Y(OH)n也一定为强碱 | |
| C. | 若X元素形成的单质是X2,则Y元素形成的单质也一定是Y2 | |
| D. | 若Y的最高正化合价为+m,则X的最高正化合价一定为+m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com