
����Ŀ������þMg(ClO3)2����������������ݼ���,ʵ�����Ʊ�����Mg(ClO3)2��6H2O���������£�
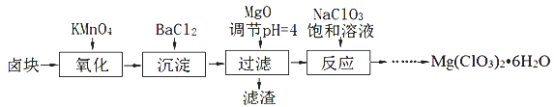
��֪����±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2�����ʡ�
�����ֻ�������ܽ��(S)���¶� (T)�仯������ͼ��ʾ��
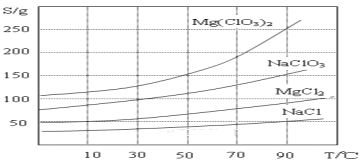
��1����������Ҫ����Ҫ����������____________��
��2������BaCl2��Ŀ����___________����MgO�����������������Ҫ�ɷ�Ϊ____________��
��3������NaClO3������Һ������Ӧ�Ļ�ѧ����ʽΪ____________��
��4���ٽ�һ����ȡMg(ClO3)2��6H2O��ʵ�鲽������Ϊ____________��
�������ᾧ���ڳ��ȹ��ˡ�ϴ�ӣ��۽���Һ��ȴ�ᾧ���ܹ��ˡ�ϴ�ӡ�
��5����Ʒ��Mg(ClO3)2��6H2O�����IJⶨ����֪Mg(ClO3)2��6H2O��Ħ������Ϊ299g/mol ��
����1��ȷ����3.50 g��Ʒ���100 mL��Һ��
����2��ȡ10.00mL��Һ����ƿ�У�����10.00mLϡ�����20.00mL1.000 mol��L��1��FeSO4��Һ���ȡ�
����3����ȴ�����£���0.100 mol/L K2Cr2O7��Һ�ζ�ʣ���Fe2+���յ㡣
�ٴ˷�Ӧ�����ӷ���ʽΪ:_____________________________________________��
����4��������2��3�ظ����Σ�ƽ������K2Cr2O7��Һ15.00 mL��
�ڲ�Ʒ��Mg(ClO3)2��6H2O����������_________________________________��
���𰸡�©�������������ձ� ��ȥSO42- �� ʹSO42-���� Fe(OH)3 MgCl2��2NaClO3��Mg(ClO3)2��2NaCl�� �٢ڢۢ� Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O 78.3%
��������
±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2������������������Ŀ���ǽ�������������Ϊ�����ӣ������Ȼ���ʹSO42-���������˳�������BaSO4������������MgO�����ᷴӦ�����κ�ˮ�����Լ���MgO�������ǵ�����Һ��pH��ʹ����Fe3+�γɳ���Fe(OH)3��ȫ��ȥ������Һ�м���NaClO3������Һ������ӦMgCl2+2NaClO3=Mg(ClO3)2+2NaCl����Ȼ����������þ���ܽ�����¶�Ӱ��仯�ϴ������Ƚ���Һ����Ũ����Ȼ���ٳ��ȹ��ˣ��Ա��ȥ���ʣ�Ȼ����ȴ�ᾧ�õ���Ҫ�IJ���Mg(ClO3)2��6H2O��
��1��������Ҫ�IJ��������У��ձ���©������������
��ȷ����©�������������ձ�
��2�������Ȼ���ʹSO42-����BaSO4�������˳�ȥ������MgO�������ǵ�����Һ��pH��ʹ����Fe3+�γ�Fe(OH)3������ȫ��ȥ��
��ȷ������ȥSO42- �� ʹSO42-������ Fe(OH)3��
��3������NaClO3������Һ������ӦMgCl2+2NaClO3=Mg(ClO3)2+2NaCl����
��ȷ����MgCl2+2NaClO3=Mg(ClO3)2+2NaCl����
��4���ٽ�һ����ȡMg(ClO3)2��6H2O��ʵ�鲽�裺����NaCl��Mg(ClO3)2���ܽ�����¶ȵĹ�ϵ����Һ����Ũ�������ȹ��ˣ���ȴ�ᾧ�����ˡ�ϴ�����õ�Mg(ClO3)2��6H2O��
��ȷ�����٢ڢۢܡ�
��5������������Ӿ��������ԣ����Խ�������������Ϊ�����ӣ���ѧ����ʽΪ��ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O�� Cr2O72-�ܽ�Fe2+������Fe3+����Ӧ�����ӷ���ʽΪCr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O��
��ȷ����Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O��
�����ݻ�ѧ����ʽ��ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O�Լ�Cr2O72-+6Fe2++14H+�T2Cr3++6Fe3++7H2O�����Եó���ClO3-��6Fe2+��Cr2O72-��6Fe2+����0.100molL-1 K2Cr2O7��Һ�ζ����յ���̿��Եó�ʣ����������ӵ����ʵ���Ϊ��0.100molL-1��0.015L��6=0.009mol����������ӷ�Ӧ���������ӵ����ʵ���Ϊ��20��10-3L��1.000molL-1-0.009mol=0.011mol����������ӵ����ʵ���Ϊ��![]() ��0.011mol����Ʒ��Mg��ClO3��26H2O��������������
��0.011mol����Ʒ��Mg��ClO3��26H2O��������������![]() ��0.011��
��0.011��![]() ��299g/mol����10��
��299g/mol����10��![]() ��100%=78.3%��
��100%=78.3%��
��ȷ����78.3% ��


 Сѧ��ѧ������ѿڶ���ϵ�д�
Сѧ��ѧ������ѿڶ���ϵ�д� ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д� �㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼװ�ý���ʵ�飬�����ƶ���ȷ����(����)
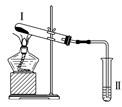
ѡ�� | �����Լ� | �����Լ������� | �ƶ� |
A | �Ȼ�� | ��̪��Һ�����ɫ | �Ȼ���ȶ� |
B | �������� | Ʒ����Һ��ɫ | FeSO4�ֽ�����FeO��SO2 |
C | Ϳ��ʯ���͵����Ƭ | ���Ը��������Һ��ɫ | ʯ���ͷ����˻�ѧ�仯 |
D | ������ˮ���� | ����ˮð�� | ������ˮ���������˷�Ӧ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����е������仯����ͼһ�µ���

A. 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
B. C+CO2![]() 2CO
2CO
C. CaCO3![]() CaO+CO2��
CaO+CO2��
D. C+H2O![]() CO+H2
CO+H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ���� 2 L ���ܱ������У����� X��Y �� Z �������ʵ����ʵ�����ʱ��仯��������ͼ��ʾ������������ȷ����
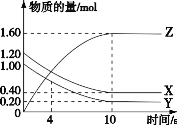
A. �����л�ѧ��ӦΪ X(g)��Y(g)![]() Z(g)
Z(g)
B. 0��10 s��X ��ʾ��ƽ����ѧ��Ӧ����Ϊ 0.04 mol/(L��s)
C. ʹ�ô���ֻ�ܼӿ� 0��10 s ��ķ�Ӧ����
D. 0��4 s ��ƽ����Ӧ����С�� 0��10 s ��ƽ����Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ϵ������ȷ����( )
A. �辧����а뵼�����ܣ������ڹ��ά
B. NH3������ˮ�������������
C. ����ͭ������ǿ������FeCl3��ʴCu����ӡˢ��·��
D. ��ˮ�еĴ�������������ԣ�����������ˮ��ɱ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. 1mol H2SO4������Ϊ98g/mol
B. ˮ��Ħ��������18g
C. ���ʵ����ȿ��Ա�ʾ���ʵ��������ֿ��Ա�ʾ���ʵ�����
D. 23g�������к��еĵ��ӵ����ʵ���Ϊ11mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǹ�[(CH3COO)2Cr��H2O��Ϊש��ɫ���壬��������ˮ���������ᣬ����������������������ռ���һ���Ʊ����������ڷ����ϵ�����ý���п����ԭ���������۸���ԭΪ���۸������۸������������Һ���ü����Ƶô����Ǹ���ʵ��װ����ͼ��ʾ���ش��������⣺

��1��ʵ������������ˮ���辭��к�Ѹ����ȴ��Ŀ����_________������a��������_______��
��2��������п�����Ȼ�����������c�У�������������ˮ����ͼ���Ӻ�װ�ã���K1��K2���ر�K3��
��c����Һ����ɫ��Ϊ����ɫ���÷�Ӧ�����ӷ���ʽΪ_________��
��ͬʱc��������������������������_____________��
��3����K3���ر�K1��K2��c������ɫ��Һ����d����ԭ����________��d������ש��ɫ������Ϊʹ����������������룬����õIJ�����___________��_________��ϴ�ӡ����
��4��ָ��װ��d���ܴ��ڵ�ȱ��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��Ϊ��ѧ��ѧ�����Ĵ����A�ǵ��ʣ���������ͼ��Ӧ��ϵ������˵���������( )

A����A�Ǵ����к����������壬C��D���������һ���ɹ⻯ѧ��Ⱦ����Dת����C�ķ�Ӧ��ѧ����Ϊ3NO2+H2O=2HNO3+2NO
B����A��B��C�ֱ�ΪC(s)��CO(g)��CO2(g)����ͨ����O2(g)��Ӧʵ��ͼʾ��ת������ͬ��ͬѹ�����ĺ�̼���ʾ�Ϊ1molʱ����Ӧ�������������ʱ�����Ϊ��H 1����H 2����H 3��������֮��Ĺ�ϵΪ ��H 2=��H 1+��H 3
C����CΪһԪǿ�������������������ĵ�������ͬ��DΪ�ճ������г��õĵ�ζƷ����ҵ����D�Ʊ�A�Ļ�ѧ����ʽ2Na2O(����)![]() 4Na+O2��
4Na+O2��
D����A��Ӧ����㷺�Ľ���������Ӧ�õ�A����������Ӧ���õ�ͬһ����̬�ǽ�������ʵ���ұ���D��Һ�ķ����Ǽ���������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ����Ƴ�ԭ��ص��ǣ� ��
A.CaCO3+2HCl�TCaCl2+H2O+CO2��B.BaCl2+Na2SO4�T2NaCl+BaSO4��
C.2NaOH+CO2�TNa2CO3+H2OD.Fe+CuCl2�TFeCl2+Cu
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com