
下列事故处理方法正确的是( )
A.汽油失火时,立即用水灭火
B.实验室不小心碰翻酒精灯引起实验桌上的少量酒精起火时,迅速用泡沫灭火器灭火
C.浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液
D.浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X最外层电子数是次外层电子数的2倍 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的非金属性大于Y |
| W | W的一种核素的质量数为23,中子数为12 |
(1)Y位于元素周期表第 周期第 族,Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写最高价氧化物对应的水化物的化学式)。
(2)W可以生成两种氧化物,分别写出这两种氧化物的电子式:_____________;__________
(3)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
XO(g)+ O2(g)=XO2(g) △H=-283.0 kJ·mol-1
O2(g)=XO2(g) △H=-283.0 kJ·mol-1
Y(g)+ O2(g)=YO2(g) △H=-296.0 kJ·mol-1
此反应的热化学方程式是 。(X、Y用实际的元素符号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A由碳、氢、氧三种元素组成。现取3 g A与4.48 L氧气(标准状况)在密闭容器中燃烧,生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过足量的浓硫酸和碱石灰,浓硫酸增重3.6 g,碱石灰增重4.4 g。回答下列问题:
(1)3 g A中所含碳原子、氢原子的物质的量各是多少? (4分)
(2)通过计算确定该有机物的分子式。 (4分)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作正确的是( )
A.用固体氯化铵和氢氧化钙制氨气结束后,将大试管从铁架台上取下立即进行洗涤
B.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出
C.做金属钠的性质实验时,剩余的钠放回原试剂瓶
D.向沸腾的NaOH稀溶液中滴入FeCl3饱和溶液,来制备Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
8g无水硫酸铜配成0.1mol/L的硫酸铜水溶液,下列说法正确的是
A.溶于500mL水中 B.溶于1L水中
C.溶解后溶液的总体积为500ml D.溶解后溶液的总体积为1L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 叙述I | 叙述II | |
| A | 水玻璃具有黏性 | 盛装烧碱溶液的试剂瓶不能用玻璃塞 |
| B | 往氯化钙溶液中通入足量的CO2 先有白色沉淀生成,后沉淀溶解 | CaCO3不溶于水,Ca(HCO3)2可溶于水 |
| C | NH4Cl受热易分解 | 可用加热法除去I2中的NH4Cl |
| D | 利用丁达尔现象区分氢氧化铁胶体和浓的氯化铁溶液 | 往氢氧化钠溶液中滴加饱和氯化铁溶液,加热至红褐色制得胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
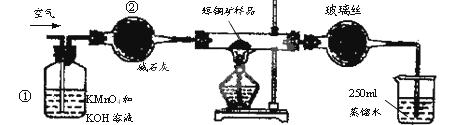
工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置。实验时按如下步骤操作:
A.连接好仪器,使其成为如图装置,并检查装置的气密性。
B.称取研细的辉铜矿样品1.000g。
C.将称量好的样品小心地放入硬质玻璃管中。
D.以每分钟1L的速率鼓入空气。
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2 SO2 +2Cu。
SO2 +2Cu。
F.移取25.00mL含SO2的水溶液于250mL锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2—3次。
试回答下列问题:
(1)装置①的作用是_________________;装置②的作用是____________________。
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为 ,当产生_______________________________的现象时可判断滴定已经达到终点。
(3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是________。
| 滴定 次数 | 待测溶液的[来源:Z.X.X.K] 体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
(4)本方案设计中由一个明显的缺陷影响了测定结果(不属于操作失误),你认为是 (写一种即可)。
(5)已知在常温下FeS 的 Ksp= 6 . 25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系:c2 (H+)·(S2-) = 1 . 0×10-22 。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为1 mol/L,应调节溶液的c(H十)为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com