
| 物质(杂质) | 试剂 | 有关离子方程式 |
| NaHCO3(Na2CO3) | ||
| FeCl2(FeCl3) |
分析 (1)①NaHCO3为强电解质,完全电离,碳酸氢根离子为弱酸酸根离子不能拆;②HClO为弱酸,在溶液中部分电离出氢离子和次氯酸根离子;
(2)Na2CO3溶液可与二氧化碳反应生成NaHCO3;FeCl3与铁反应生成FeCl2,以此除杂;
(3)镁条点燃后在二氧化碳气体中继续燃烧生成氧化镁和碳;
(4)CO32-+2H+=CO2↑+H2O可表示可溶性碳酸盐和强酸反应生成可溶性盐和二氧化碳和水.
解答 解:(1)①NaHCO3为强电解质,完全电离,电离方程式为:NaHCO3=Na++HCO3-;
故答案为:NaHCO3=Na++HCO3-;
②HClO为弱酸,在溶液中部分电离出氢离子和次氯酸根离子,其电离方程式为:HClO?H++ClO-;
故答案为:HClO?H++ClO-;
(2)Na2CO3溶液可与二氧化碳反应生成NaHCO3,反应的方程式为Na2CO3+H2O+CO2=2NaHCO3,离子方程式为:CO32-+CO2+H2O=2HCO3-,FeCl3与铁反应生成FeCl2,反应的化学方程式为2FeCl3+Fe═3 FeCl2,离子方程式为:Fe+2Fe3+=3Fe2+,
故答案为:
| 物质(杂质) | 试剂 | 有关离子方程式 |
| NaHCO3(Na2CO3) | CO2 | CO32-+CO2+H2O=2HCO3- |
| FeCl2(FeCl3) | Fe | Fe+2Fe3+=3Fe2+ |
点评 本题考查方程式书写、混合物分离提纯以及物质的检验和鉴别,为高频考点,分离提纯注意把握物质的性质及混合物分离方法、原理为解答的关键,题目难度中等.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:选择题
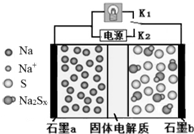 高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )
高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )| A. | 放电时,石墨电极a为正极 | |
| B. | 放电时,Na+从石墨b向石墨a方向迁移 | |
| C. | 可将装置中的固体电解质改成NaCl溶液 | |
| D. | 充电时,b极反应为Na2Sx-2e-=xS+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | 1 | 2 | 3 |
| V(盐酸)/mL | 50 | 50 | 50 |
| m(混合物)/g | 9.2 | 15.7 | 27.6 |
| V(CO2)(标准状况)/L | 2.24 | 3.36 | 3.36 |
| A. | 实验②中,混合物过量 | |
| B. | 原混合物样品中n(NaHCO3):n(KHCO3)=1:1 | |
| C. | 盐酸的物质的量浓度为2mol•L-1 | |
| D. | 实验反应后,至少需继续加入50mL的盐酸溶液才能使27.6g的混合物全部反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学欲做1-氯丁烷的水解实验,并检验其中的氯元素.实验过程如下:(如图所示)在大试管中加入5mL 1mol•L-1 NaOH溶液和5mL的1-氯丁烷(1-氯丁烷的沸点为77~78℃,密度为0.886g•cm-3,易燃).水浴加热该试管10min以上,并控制加热温度在70~80℃.取两支小试管,各加入约1mL由2%的AgNO3和3mol•L-1硝酸按1:1比例组成的混合溶液,用胶头滴管吸取加热后大试管内的上层溶液,将此待测液逐滴加入其中一支小试管中,与另一支未加待测液的小试管内溶液相比,有白色的浑浊物出现,说明1-氯丁烷与NaOH溶液反应有Cl-生成,从而证明了1-氯丁烷中含有氯元素.请回答:
某同学欲做1-氯丁烷的水解实验,并检验其中的氯元素.实验过程如下:(如图所示)在大试管中加入5mL 1mol•L-1 NaOH溶液和5mL的1-氯丁烷(1-氯丁烷的沸点为77~78℃,密度为0.886g•cm-3,易燃).水浴加热该试管10min以上,并控制加热温度在70~80℃.取两支小试管,各加入约1mL由2%的AgNO3和3mol•L-1硝酸按1:1比例组成的混合溶液,用胶头滴管吸取加热后大试管内的上层溶液,将此待测液逐滴加入其中一支小试管中,与另一支未加待测液的小试管内溶液相比,有白色的浑浊物出现,说明1-氯丁烷与NaOH溶液反应有Cl-生成,从而证明了1-氯丁烷中含有氯元素.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
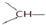 和一个-OH,它的可能结构式有( )
和一个-OH,它的可能结构式有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向盐酸中滴加氨水:H++OH-═H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| D. | 向次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | |
| C. | 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏 | |
| D. | 除去甲烷中混有的少量乙烯:将混合气体通入酸性KMnO4溶液中洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 | |
| B. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| C. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com