
 铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体不同温度下转化的图示,下列有关说法不正确的是( )
铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体不同温度下转化的图示,下列有关说法不正确的是( )| A. | δ-Fe晶体中与相邻铁原子距离相等且最近的铁原子有8个 | |
| B. | γ-Fe晶体中与相邻铁原子距离相等且最近的铁原子有12个 | |
| C. | α-Fe晶胞边长若为a cm,y-Fe晶胞边长若为b cm,则a-Fe和y-Fe两种晶体的 密度比为b3:a3 | |
| D. | 将铁加热到1500℃后分别急速冷却和缓慢冷却,得到的晶体类型不同 |
分析 A.根据δ-Fe晶体晶胞类型判断配位数;
B.根据γ-Fe晶体晶胞类型判断配位数;
C.计算两种晶胞的密度之比;
D.加热到1500℃急速冷却得到δ-Fe晶体,缓慢冷却得到α-Fe晶体,据此判断.
解答 解:A.δ-Fe晶体晶胞类型为体心立方,与位于体心的Fe原子,距离最近的Fe原子位于顶点,共有8个,则配位数为8,故A正确;
B.γ-Fe晶体晶胞类型为面心立方,位于顶点的Fe原子,被晶胞的三个平面共有,每个平面与其距离相等的Fe原子数目为4,则共有3×4=12,故配位数为12,故B正确;
C.若α-Fe晶胞边长为acm,γ-Fe晶胞边长为bcm,则两种晶体中铁原子个数之比=(8×$\frac{1}{8}$):(8×$\frac{1}{8}$+6×$\frac{1}{2}$)=1:4,密度比=$\frac{\frac{56}{{N}_{A}}}{{a}^{3}}$:$\frac{\frac{56×4}{{N}_{A}}}{{b}^{3}}$=b3:4a3,故C错误;
D.将铁加热到1500℃分别急速冷却和缓慢冷却,温度不同,得到的晶体类型不相同,故D正确;
故选C.
点评 本题考查不同晶胞类型的配位数和晶胞结构计算,难度不大,应熟练掌握晶胞密度的计算方式.


科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | 大气固氮 N2 (g)+O2 (g)?2NO(g) | 工业固氮 N2 (g)+3H2 (g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +H2O
+H2O
 ;E中含氧官能团的名称:羧基.
;E中含氧官能团的名称:羧基. +
+ $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.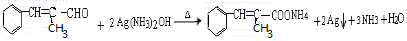 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=Q2=197 | B. | Q1=Q2<197 | C. | Q1<Q2<197 | D. | Q2<Q1<197 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 等物质的量的甲烷和乙酸完全燃烧消耗氧气的量相等 | |
| C. | 把溴水分别加到足量NaOH溶液和己烯中,充分反应后溶液都呈无色,所以不能用溴水鉴别这两种物质 | |
| D. | 检验某溶液中是否含有乙醛:在盛有2 mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热,看是否产生砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 顺序 | 步骤 | 实验现象 |
| ① | 取少量纯净的NaCl,加蒸馏水溶解 | 溶液无变化 |
| ② | 滴加淀粉KI溶液,振荡 | 溶液无变化 |
| ③ | 然后再滴加稀H2SO4溶液,振荡 | 溶液变蓝色 |
| 实验操作 | 实验现象及结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com