
| A. | 因为s轨道的形式是球形的,所以处于s轨道上的电子做的是圆周运动 | |
| B. | 电子在3px、3py、3ps三个轨道上运动时,能量不同 | |
| C. | 电子云是用来形象的描述电子运动状态的 | |
| D. | H、F、Cl、O的电负性逐渐增大 |
分析 A.电子云轮廓图称为原子轨道,S轨道的形状是球形的,表示电子出现概率大小;
B.同一能级中的电子能量相同;
C.电子云就是用小黑点疏密来表示空间各电子出现概率大小的一种图形;
D.电负性表示对键合电子的吸引力,电负性越大对键合电子吸引力越大,所以非金属性越强电负性越强,同周期元素从左到右元素的电负性依次增大,同主族自上而下电负性减小.
解答 解:A.S轨道的形状是球形的,表示电子出现概率大小,而不表示电子运动轨迹,故A错误;
B.3px、3py、3pz属于同一能级上的电子,其能量相同,故B错误;
C.电子云不是笼罩在原子核外的雨雾,是表示电子出现的几率,用来描述电子运动状态,小黑点的疏密表示电子在原子核外单位体积内出现机会的大小,故C正确;
D.O、F处于同一周期,同周期自左而右电负性增大,故电负性O<F,F、Cl同主族,自上而下电负性减小,故电负性Cl<F,非金属性越强电负性越强,所以H、Cl、O、F的电负性逐渐增大,故D错误;
故选C.
点评 本题考查轨道、电子云、电负性等知识点,易错选项是B,注意同一能级上电子能量相同,明确电子云含义,为易错点,注意元素电负性大小判断技巧,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 航天服材质是由碳化硅/陶瓷和碳纤维等复合而成,具有耐高温防寒等性能 | |
| B. | 从海水提取物质不一定都必须通过化学反应才能实现 | |
| C. | 二氧化硅可用于制备太阳能电池板,晶体硅可用于制作光导纤维 | |
| D. | 明矾可用于自来水的净化,氯气可用于自来水的杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
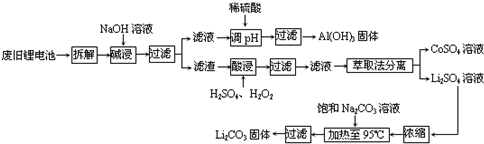
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
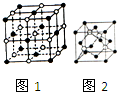 钠和铜的单质及其化合物在生活实际中有着广泛的应用.
钠和铜的单质及其化合物在生活实际中有着广泛的应用.| NaF | NaCl | NaBr | NaI | |
| 熔点/℃ | 993 | 801 | 747 | 661 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
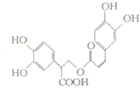 迷迭香酸是从蜂花属植物中提取的物质,其结构简式如图所示.则等量的迷迭香酸消耗的Br2、NaOH、NaHCO3的物质的量之比为( )
迷迭香酸是从蜂花属植物中提取的物质,其结构简式如图所示.则等量的迷迭香酸消耗的Br2、NaOH、NaHCO3的物质的量之比为( )| A. | 7:6:1 | B. | 7:6:5 | C. | 6:7:1 | D. | 6:7:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| C. | 等量H2在O2中完全燃烧生成H2O(g)与生成H2O(l),前者放出的热量多 | |
| D. | 在101 kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小顺序:r(W)>r(Y)>r(X) | |
| B. | 非金属性强弱顺序:X>W>Z | |
| C. | 最高价氧化物对应水化物的酸性:Z>W | |
| D. | 化合物Y2X、ZX2、WX3中化学键类型相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com