
| A. | 工业上可通过电解熔融的AlCl3来得到金属铝 | |
| B. | 电解饱和食盐水制氯气可采用铁作为阳极 | |
| C. | 炒菜铁锅易生锈是因为形成了原电池,铁作负极 | |
| D. | 工业上一般采用铝热法冶炼金属镁 |
分析 A、氯化铝为共价化合物,熔融氯化铝不导电;
B、Fe是活性电极,电解池中作阳极时,Fe电极放电;
C、Fe中含有C,在潮湿的空气中形成原电池,加快腐蚀速度;
D、Mg比Al活泼,不能用Al冶炼Mg.
解答 解:A、氯化铝属于共价化合物,熔融氯化铝不导电,则无法电解熔融氯化铝,工业上是通过电解熔融氧化铝的方法获得铝,故A错误;
B、电解池中Fe作阳极时,Fe电极放电,不能生成氯气,故B错误;
C、Fe在潮湿的空气中形成原电池,加快腐蚀速度,活泼金属Fe作负极,故C正确;
D、铝热法冶炼的金属熔点较高且不如Al活泼,Mg比Al活泼,不能用Al冶炼Mg,故D错误;
故选C.
点评 本题考查了电解池原理,注意氯化铝是共价化合物,熔融状态下不导电,题目难度不大.


 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:选择题
| A. | 任何反应都伴有能量的变化 | |
| B. | 化学反应中的能量变化可表现为热量的变化 | |
| C. | 反应物的总能量高于生成物的总能量时,发生吸热反应 | |
| D. | 反应物的总能量低于生成物的总能量时,发生吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
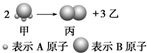 如图所示:已知甲、乙、丙常温下都为气体.2mol甲分子反应生成1mol丙和3mol乙,
如图所示:已知甲、乙、丙常温下都为气体.2mol甲分子反应生成1mol丙和3mol乙,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠是银白色金属,质软,熔点相对较低,密度比水小 | |
| B. | 大量的钠着火时可以用沙扑灭,不能用水或泡沫灭火剂灭火 | |
| C. | 金属钠在空气中长期放置,最终变为碳酸钠 | |
| D. | Na2O和Na2O2都能由金属钠和氧气化合生成,Na2O和Na2O2氧的价态也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
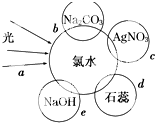 氯气是一种重要的化工原料.
氯气是一种重要的化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲烷中的氢原子被氯原子完全取代,需要2NACl | |
| B. | 1mol•L-1Mg(NO3)溶液中含有NO3-的数目为2NA | |
| C. | 标准状况下.22.4LBr2中所含的分子数为NA | |
| D. | Na2O2与水反应时,每生成0.1 molO2,转移电子的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com