
 CO(g)��H2(g)��5 min�ﵽƽ����ܶ�������0.3 g��L��1���й�����˵����ȷ����
CO(g)��H2(g)��5 min�ﵽƽ����ܶ�������0.3 g��L��1���й�����˵����ȷ����| A���ӷ�Ӧ��ʼ��ƽ������У���C����ʾ�÷�Ӧ��ƽ������Ϊ0.005 mol��L��1��min��1 |
| B����ƽ��ʱѹǿ��Ϊԭ����7/6 |
| C�����¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ0.005 |
| D���������¶Ⱥ�������䣬��ƽ����ϵ���ټ���0.2 mol C(s)��0.3 mol H2O(g)�����´ﵽƽ���H2O��ת���ʵ���16.7% |
 CO(g)��H2(g)��֪���ӵ��������Dzμӷ�Ӧ��̼�����������ʵ�����0.6g��12g/mol��0.05mol����
CO(g)��H2(g)��֪���ӵ��������Dzμӷ�Ӧ��̼�����������ʵ�����0.6g��12g/mol��0.05mol���� CO(g)��H2(g)
CO(g)��H2(g)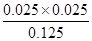 ��0.005��C��ȷ��
��0.005��C��ȷ��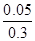 ��100%��16.67%��D����ȷ����ѡBC��
��100%��16.67%��D����ȷ����ѡBC��

 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д� Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ת��Ϊ���� |
| B����ѧ��ת��Ϊ���� |
| C������������������ڷ�Ӧ��������� |
| D������������������ڷ�Ӧ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���ڢۢ� | C���٢� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ʵ���ò�ͬ�¶��µ�ƽ�����������±���
ʵ���ò�ͬ�¶��µ�ƽ�����������±���
| A��2v(NH3)=v(C02)���������������� | B���ܱ���������ѹǿ���� |
| C���ܱ������л��������ܶȲ��� | D���ܱ������а���������������� |
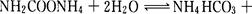
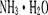 ���о�С��ֱ������ݲ�ͬ��ʼŨ�ȵİ����������Һ�ⶨˮ�ⷴӦ���ʣ��õ�C(NH2C00-)��ʱ��ı仯������ͼ��ʾ��
���о�С��ֱ������ݲ�ͬ��ʼŨ�ȵİ����������Һ�ⶨˮ�ⷴӦ���ʣ��õ�C(NH2C00-)��ʱ��ı仯������ͼ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
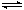 Y(g)+Z(g) ��H��0����Ӧ��8minʱ�ﵽƽ�⣻��14minʱ�ı���ϵ���¶ȣ� 16minʱ������ƽ�⡣X�����ʵ���Ũ�ȱ仯��ͼ��ʾ�������й�˵����ȷ����
Y(g)+Z(g) ��H��0����Ӧ��8minʱ�ﵽƽ�⣻��14minʱ�ı���ϵ���¶ȣ� 16minʱ������ƽ�⡣X�����ʵ���Ũ�ȱ仯��ͼ��ʾ�������й�˵����ȷ����
| A��0��8min��Y��ʾ�÷�Ӧ����Ϊ0.1mol��L-1��min��1 |
| B��8minʱ�ﵽƽ�⣬�÷�Ӧ��ƽ�ⳣ��ΪK= 0.5 |
| C��14minʱ���ı�ķ�Ӧ���ǽ������¶� |
| D��16minʱ������Ӧ���ʱ�8minʱ������Ӧ���ʴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ѧ��Ӧ���ʱ�ʾ���ǻ�ѧ��Ӧ���е��� |
| B����ѧ��Ӧ���ʿ����õ�λʱ���ڷ�Ӧ��Ũ�ȵļ���������ʾ |
| C�������κλ�ѧ��Ӧ��˵����Ӧ����Խ�죬��Ӧ�����Խ���� |
| D����ѧ��Ӧ���ʿ�������ֵ��Ҳ�����Ǹ�ֵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

| ���� | HCOOH | CH3OH | HCOOCH3 |
| ��Ҫ ���� | ��ɫҺ�壬��ˮ���� K(HCOOH)>K(CH3COOH) | ��ɫҺ�壬��ˮ���� | ��ɫҺ�壬��ˮ���ܽ��С���봼���� |
 HCOOH(l) + CH3OH(l)����Ӧ���ȣ����ʱ��ֵ��С�����³�ѹ�£�ˮ�ⷴӦ���ʺ�ƽ�ⳣ������С��
HCOOH(l) + CH3OH(l)����Ӧ���ȣ����ʱ��ֵ��С�����³�ѹ�£�ˮ�ⷴӦ���ʺ�ƽ�ⳣ������С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 M(g)��N(g)������ʵ���������±���
M(g)��N(g)������ʵ���������±���| ʵ�� ��� | �¶�/�� | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | |
| n(X) | n(Y) | n(M) | ||
| �� | 700 | 0.40 | 0.10 | 0.090 |
| �� | 800 | 0.10 | 0.40 | 0.080 |
| �� | 800 | 0.20 | 0.30 | a |
| �� | 900 | 0.10 | 0.15 | b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��ͼ�ٱ�ʾһ��������ij��ѧ��Ӧ��������ʱ��仯������ͼ���÷�Ӧһ��Ϊ���ȷ�Ӧ |
| B��ͼ�ڱ�ʾ�����ǻ�����������Һ�м������ᣬ���������������仯 |
| C��ͼ�۱�ʾ������������ʵ���Ũ�ȵ�����ʹ�����Һ���ֱ��������þ�ۣ�����H2�����ʵ����ı仯 |
| D��ͼ��Ϊˮ�ĵ���ƽ������ͼ������A�㵽C�㣬�ɲ�����ˮ�м�������NaOH����ķ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com