
(1)已知:25℃时,一些弱电解质的电离常数如下:NH3·H2O:1.77×10—5 H2CO3:4.3×10—7(第一步电离)。则:NH4HCO3溶液显 性 。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 性,醋酸体积 (填“>”、“<”、“=”)氢氧化钠溶液体积。
(3)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=10,A溶液呈碱性的原因是(用离子方式程式表示)________________
(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是: ;有人认为加入FeS作为沉淀剂还可以起到净化水的作用,请您运用所学知识解释
(5)已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10—15。在AB2、AC均为饱和的混合液中,测得c(B—)=1.6×10—3 mol·L-1,则溶液中c(C2—)为 mol/L。
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)(1)已知在25℃时:①2CO (s)+ O2 (g)==2CO2 (g) △H1=-566KJ/mol
②C (s)+O2(g)==CO2 (g) △H2=-394KJ/mol,则碳与氧气反应生成一氧化碳的热化学方程式为:__________________________________________________;
(2)在体积为2 L的密闭容器中,A与B在一定条件下反应生成C:
A (g)+2B (s) 2C (g)。反应达到平衡时,平衡常数表达式K= _______ ;在不同温度下达到平衡时生成物C的物质的量如下图所示,则该反应是 反应(填“放热”或“吸热” )。在500℃,从反应开始到平衡,C的平均反应速率v(C) = 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年云南省昆明三中、滇池中学高二下学期期末考试化学卷(带解析) 题型:填空题
(1)已知:25℃时,一些弱电解质的电离常数如下:NH3·H2O:1.77×10—5 H2CO3:4.3×10—7(第一步电离)。则:NH4HCO3溶液显 性 。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 性,醋酸体积 (填“>”、“<”、“=”)氢氧化钠溶液体积。
(3)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=10,A溶液呈碱性的原因是(用离子方式程式表示)________________
(4)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是: ;有人认为加入FeS作为沉淀剂还可以起到净化水的作用,请您运用所学知识解释
(5)已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10—15。在AB2、AC均为饱和的混合液中,测得c(B—)=1.6×10—3 mol·L-1,则溶液中c(C2—)为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2013届福建省三明一中、二中高三上学期期末联考化学试卷(带解析) 题型:填空题
运用化学反应原理研究氢、氧、氯、碘等单质及其化合物的反应有重要意义
(1)已知:25℃时KSP(AgCl)=1.6×l0-10 KSP(AgI)=1.5×l0-16
海水中含有大量的元素,常量元素如氯,微量元素如碘,其在海水中均以化合态存在。在25℃下,向0.1L0.002mol·L-l的NaCl溶液中加入0.1L0.002mol·L-l硝酸银溶液,有白色沉淀生成,产生沉淀的原因是(通过计算回答) ,向反应后的浑浊液中继续加入0.1L0.002mol·L-1的NaI溶液,看到的现象是 ,产生该现象的原因是(用离子方程式表示) 。
(2)过氧化氢的制备方法很多,下列方法中原子利用率最高的是 (填序号)。
A.BaO2 + H2SO4= BaSO4 ↓ + H2O2
B.2NH4HSO4 (NH4)2S2O8 + H2↑
(NH4)2S2O8 + H2↑
(NH4)2S2O8 + 2H2O = 2NH4HSO4 + H2O2
C.CH3CHOHCH3 + O2→ CH3COCH3 + H2O2
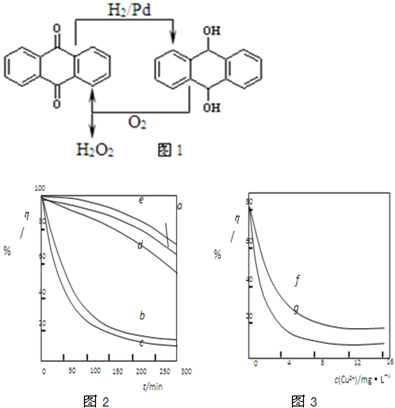
D.乙基蒽醌法见下图
(3)某文献报导了不同金属离子及其浓度对双氧水氧化降解海藻酸钠溶液反应速率的影响,实验结果如图1、图2所示。
注:以上实验均在温度为20℃、w(H2O2)=0.25%、pH=7.12、海藻酸钠溶液浓度为8mg·L―1的条件下进行。图1中曲线a:H2O2;b:H2O2+Cu2+;c:H2O2+Fe2+;d:H2O2+Zn2+;e:H2O2+Mn2+;图2中曲线f:反应时间为1h;g:反应时间为2h;两图中的纵坐标代表海藻酸钠溶液的粘度(海藻酸钠浓度与溶液粘度正相关)。
由上述信息可知,下列叙述错误的是 (填序号)。
A.锰离子能使该降解反应速率减缓
B.亚铁离子对该降解反应的催化效率比铜离子低
C.海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢
D.一定条件下,铜离子浓度一定时,反应时间越长,海藻酸钠溶液浓度越小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com