
 ��
�� ��
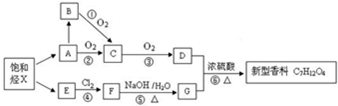
������ ������X������̼��������Ϊ24��5����̼�������Ϊ$\frac{24}{12}$��$\frac{5}{1}$=2��5������X�ķ���ʽΪC4H10��X����Ϊֱ���ṹ������XΪCH3CH2CH2CH3��A��E����X���ѽ����Ҷ���Ϊͬϵ���A��EΪ��ϩ�ͱ�ϩ��D�뱥��NaHCO3��Һ��Ӧ�������壬��DΪ���ᣬE�������ӳɵ�F��Fˮ���G����GΪ��Ԫ���������������ϵķ���ʽ��֪��������Ϊ��Ԫ�������Ը���̼ԭ���غ㣬G��Ӧ������̼��D��Ӧ������̼������AΪ��ϩ��EΪ��ϩ������ת����ϵ��֪��BΪCH3CH2OH��CΪCH3CHO��DΪCH3COOH��FΪCH3CHClCH2Cl��GΪCH3CHOHCH2OH��A������C��B������C��C������D��E�����ӳɵ�F��F����ȡ����G��G��D����������ȡ���������ϣ��Դ˽����⣮
��� �⣺������X������̼��������Ϊ24��5����̼�������Ϊ$\frac{24}{12}$��$\frac{5}{1}$=2��5������X�ķ���ʽΪC4H10��X����Ϊֱ���ṹ������XΪCH3CH2CH2CH3��A��E����X���ѽ����Ҷ���Ϊͬϵ���A��EΪ��ϩ�ͱ�ϩ��D�뱥��NaHCO3��Һ��Ӧ�������壬��DΪ���ᣬE�������ӳɵ�F��Fˮ���G����GΪ��Ԫ���������������ϵķ���ʽ��֪��������Ϊ��Ԫ�������Ը���̼ԭ���غ㣬G��Ӧ������̼��D��Ӧ������̼������AΪ��ϩ��EΪ��ϩ������ת����ϵ��֪��BΪCH3CH2OH��CΪCH3CHO��DΪCH3COOH��FΪCH3CHClCH2Cl��GΪCH3CHOHCH2OH��A������C��B������C��C������D��E�����ӳɵ�F��F����ȡ����G��G��D����������ȡ���������ϣ�
��1����������ķ�����XΪCH3CH2CH2CH3��GΪCH3CHOHCH2OH�����еĹ�����Ϊ-OH���ʴ�Ϊ��CH3CH2CH2CH3��-OH��
��2��EΪCH3CH=CH2������3��H����һ�ȴ�����3�֣�FΪCH3CHClCH2Cl��GΪCH3CHOHCH2OH��F����ȡ����Ӧ����G���ʴ�Ϊ��3��ȡ����Ӧ��
��3�����Ļ�ѧ��Ӧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
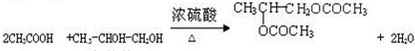
��4��B��D��Ũ���������£����ɼ�ΪCH3COOCH2CH3�������ͬ����ͬ���칹�����CH3CH2COOCH3��HCOOCH2CH2CH3��HCOOCH��CH3��2����3 �֣��������ף���
�ʴ�Ϊ��3��
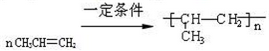
��5��EΪ��ϩ��E���ܷ����Ӿ۷�Ӧ����Ӧ�ķ���ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϡ��л���ṹ�����ʣ�Ϊ�߿��������ͣ�������ѧ���ķ��������Ŀ��飬��Ŀ�漰ϩ��������ȩ������������ת���ȣ�����Ĺؼ���A��E��ȷ�����ѶȲ��������ڻ���֪ʶ�Ĺ��̣�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2+O2�T2H2O��H=-571.6KJ/mol | |
| B�� | H2 ��g��+$\frac{1}{2}$O2��g���TH2O ��l����H=-142.9KJ/mol | |
| C�� | H2 ��g��+$\frac{1}{2}$O2��g���TH2O ��l����H=-285.8KJ/mol | |
| D�� | 2H2��g��+O2��g���T2H2O ��g����H=-571.6KJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 �� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڶ����ڢ�A�� | B�� | �������ڢ�A�� | C�� | �������ڢ�A�� | D�� | �ڶ����ڢ�A�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| 0.01mol•L-1 KIO3 ������Һ�������ۣ������/mL | 0.01mol•L-1 Na2SO3 ��Һ�����/mL | H2O����� /mL | ʵ�� �¶� /�� | ��Һ������ɫʱ����ʱ��/s | |
| ʵ��1 | 5 | V1 | 35 | 25 | |
| ʵ��2 | 5 | 5 | 40 | 25 | |
| ʵ��3 | 5 | 5 | V2 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������ᣩ�������Ҵ���Ũ���ᣬȻ����� | |
| B�� | ̼���ƹ��壨̼�����ƣ������������� | |
| C�� | FeCl2��Һ��FeCl3��CuCl2�����������Fe�۳�ֽ��裬Ȼ����� | |
| D�� | �Ҵ���ˮ�����������Ƶ���ʯ�ң�Ȼ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
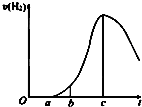 �ɶ�������������С������˹��ڡ����ý������ᷴӦ����ʵ�飬�ó���һЩ��Ȥ���뷨������������ǣ����һЩ�жϣ���5.4g��ƬͶ��500mL 0.5mol•L-1��������Һ�У���ͼΪ��Ӧ���������뷴Ӧʱ��Ĺ�ϵͼ��
�ɶ�������������С������˹��ڡ����ý������ᷴӦ����ʵ�飬�ó���һЩ��Ȥ���뷨������������ǣ����һЩ�жϣ���5.4g��ƬͶ��500mL 0.5mol•L-1��������Һ�У���ͼΪ��Ӧ���������뷴Ӧʱ��Ĺ�ϵͼ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com