
分析 ①在无机非金属材料中,硅及其化合物是密切联系生产生活的一类重要物质,陶瓷、玻璃、水泥等都是硅酸盐产品属于硅酸盐材料,据此分析;
②防止金属腐蚀的方法有:牺牲阳极的阴极保护法、外加电源的阴极保护法、改变物质结构、涂油等,据此分析解答;
③根据制取水泥、玻璃的生产中使用的原料来解答.
解答 解:①硅酸盐产品主要有陶瓷、玻璃、水泥等,青铜属于合金,沥青属于有机物,不是硅酸盐,
故选b;
②a.在钢铁制品表面镀一层金属锌,采用的是牺牲阳极的阴极保护法,所以能防止或减缓钢铁腐蚀,故a不符合;
b.在钢铁中加入锰、铬等金属,以改变钢铁结构,使用不锈钢,能防止或减缓钢铁腐蚀,故b不符合;
c.把钢铁雕塑焊接在铜质基座上,则金属铁做原电池的负极,会加快腐蚀速率,故c错误;
故选c;
③制取水泥的主要原料为黏土、石灰石、石膏等,制备普通玻璃的主要原料为纯碱、石灰石、石英等,所以制取水泥、玻璃共同使用的主要原料是石灰石,
故选a.
点评 本题考查硅酸盐材料的判别、金属的腐蚀与防护、制造玻璃和水泥的主要原料,掌握相关的基础知识是解本题关键,题目难度不大.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=4的醋酸中:c(H+)=4.0mol•L-1 | |
| B. | 饱和小苏打溶液中:c(Na+)>c(HCO3-) | |
| C. | 饱和食盐水中:c(Na+)+c(H+)=c(Cl-) | |
| D. | pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{1}^{1}$H和${\;}_{1}^{2}$H | B. | 金刚石和石墨 | ||
| C. | CH3CH2OH和CH3OCH3 | D. | CH4和C2H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2的电子式: | |
| B. | 乙酸的结构简式:C2H4O2 | |
| C. | S2-的结构示意图: | |
| D. | 氢氧化钡的电离方程式:Ba(OH)2═Ba2+(OH)${\;}_{2}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
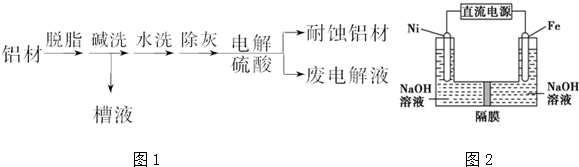
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3+3CO=═2Fe+3CO2△H=-28.5 kJ•mol-1 | |
| B. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-28.5 kJ | |
| C. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=+28.5 kJ•mol-1 | |
| D. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PO43- | B. | CCl4 | C. | NO3- | D. | SiH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时,立即用水灭火 | |
| B. | 配制稀硫酸时将水倒入浓硫酸中 | |
| C. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处走 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com